INSULIN : MEKANISME SEKRESI DAN ASPEK METABOLISME
Proses Pembentukan dan Sekresi Insulin
Hormon adalah zat kimia yang terbentuk dalam satu organ atau bagian tubuh dan dibawa dalam darah ke organ atau bagian di mana mereka menghasilkan efek fungsional. Hormon membawa pesan dari kelenjar kepada sel-sel untuk mempertahankan tingkat bahan kimia dalam aliran darah yang mencapai homeostasis. Insulin merupakan hormon yang terdiri dari rangkaian asam amino, dihasilkan oleh sel beta kelenjar pankreas. Dalam keadaan normal, bila ada rangsangan pada sel beta, insulin disintesis dan kemudian disekresikan kedalam darah sesuai kebutuhan tubuh untuk keperluan regulasi glukosa darah. Secara fisiologis, regulasi glukosa darah yang baik diatur bersama dengan hormone glukagon yang disekresikan oleh sel alfa kelenjar pankreas.
Insulin merupakan sejenis hormon peptida yang dihasilkan oleh sel beta dari Langerhans pankreas. Sel beta adalah sejenis sel yang terdapat dalam kelompok sel yang digelar membentuk pepulau (islet of) Langerhans dalam pankreas. Fungsi utama insulin ialah pengawalan keseimbangan tahap glukosa dalam darah dan bertindak meningkatkan pengambilan glukosa oleh sel badan. Kegagalan badan untuk menghasilkan insulin akan menyebabkan glukosa tidak dapat masuk ke dalam dan digunakan oleh sel-sel tubuh. Peningkatan glukosa dalam darah akan menyebabkan penyakit kencing manis yang dikenal sebagai diabetes melitus.
Aspek penting dari kerja hormon insulin pada hepar adalah insulin akan menekan peran pelepasan glukosa endogen dari hepar apabila kadar glukosa dalam darah meningkat sehingga kadar glukosa dalam darah tidak bertambah banyak. Seperti kita tahu keadaan homeostasis (normal) glukosa tubuh juga turut dipertahankan oleh hepar. Ketika kadar glukosa dalam darah menurun dari ambang normal maka hepar akan melakukan proses glukoneogenesis dan glikogenolisis menghasilkan glukosa endogen yang dikeluarkan ke dalam darah untuk meningkatkan kadarnya menuju batas normal. Apabila kadar glukosa dalam darah sudah tinggi dan insulin terstimulasi untuk keluar maka kerjanya pada hepar menyebabkan hepar tidak mensekresikan glukosa endogen lagi, sehingga kadar glukosa tidak bertambah tinggi.
Sintesis insulin dimulai dalam bentuk preproinsulin (precursor hormon insulin) pada retikulum endoplasma sel beta. Dengan bantuan enzim peptidase, preproinsulin mengalami pemecahan sehingga terbentuk proinsulin, yang kemudian dihimpun dalam gelembung-gelembung (secretory vesicles) dalam sel tersebut. Di sini, sekali lagi dengan bantuan enzim peptidase, proinsulin diurai menjadi insulin dan peptida-C (C-peptide) yang keduanya sudah siap untuk disekresikan secara bersamaan melalui membran sel.
Sekresi insulin adalah proses yang membutuhkan energi dan melibatkan sistem mikrotubulus mikrofilamen dalam sel β pulau Langerhans. Sejumlah perantara (mediator) terlibat dalam proses pelepasan insulin. Mekanisme diatas diperlukan bagi berlangsungnya proses metabolisme secara normal, karena fungsi insulin memang sangat dibutuhkan dalam proses utilisasi glukosa yang ada dalam darah. Kadar glukosa darah yang meningkat, merupakan komponen utama yang memberi rangsangan terhadap sel beta dalam memproduksi insulin. Disamping glukosa, beberapa jenis asam amino dan obat-obatan, dapat pula memiliki efek yang sama dalam rangsangan terhadap sel beta. Mengenai bagaimana mekanisme sesungguhnya dari sintesis dan sekresi insulin setelah adanya rangsangan tersebut, merupakan hal yang cukup rumit dan belum sepenuhnya dapat dipahami secara jelas.
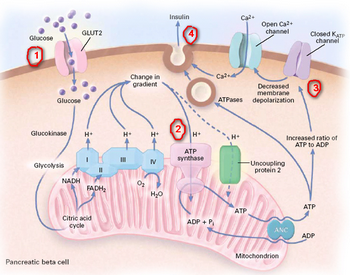
Diketahui ada beberapa tahapan dalam proses sekresi insulin, setelah adanya rangsangan oleh molekul glukosa. Tahap pertama adalah proses glukosa melewati membrane sel. Untuk dapat melewati membran sel beta dibutuhkan bantuan senyawa lain. Glucose transporter (GLUT) adalah senyawa asam amino yang terdapat di dalam berbagai sel yang berperan dalam proses metabolisme glukosa. Fungsinya sebagai “kendaraan” pengangkut glukosa masuk dari luar kedalam sel jaringan tubuh. Glukosa masuk ke dalam sel secara difusi dengan bantuan GLUT-2 glucose transporter. Glucose transporter 2 (GLUT 2) yang terdapat dalam sel beta misalnya, diperlukan dalam proses masuknya glukosa dari dalam darah, melewati membran, ke dalam sel. Proses ini penting bagi tahapan selanjutnya yakni molekul glukosa akan mengalami proses glikolisis dan fosforilasi didalam sel dan kemudian membebaskan molekul ATP. Molekul ATP yang terbentuk, dibutuhkan untuk tahap selanjutnya yakni proses mengaktifkan penutupan K channel pada membran sel. Penutupan ini berakibat terhambatnya pengeluaran ion K dari dalam sel yang menyebabkan terjadinya tahap depolarisasi membran sel, yang diikuti kemudian oleh tahap pembukaan Ca channel. Keadaan inilah yang memungkinkan masuknya ion Ca ke dalam sel β sehingga menyebabkan peningkatan kadar ion Ca intrasel dan memicu exocytosis insulin. Selanjutnya molekul insulin masuk ke dalam sirkulasi darah terikat dengan reseptor. Ikatan insulin dan reseptornya membutuhkan GLUT-4 glucose transporter untuk dapat masuk ke dalam sel otot danjaringan lemak, serta uptake glukosa dengan efisien, yang akhirnya menurunkan kadar glukosa dalam plasma
Seperti disinggung di atas, terjadinya aktivasi penutupan K channel tidak hanya disebabkan oleh rangsangan ATP hasil proses fosforilasi glukosa intrasel, tapi juga dapat oleh pengaruh beberapa faktor lain termasuk obat-obatan. Namun senyawa obat-obatan tersebut, misalnya obat anti diabetes sulfonil urea, bekerja pada reseptor tersendiri, tidak pada reseptor yang sama dengan glukosa, yang disebut sulphonylurea receptor (SUR) pada membran sel beta.
Dinamika Sekresi Insulin
Dalam keadaan fisiologis, insulin disekresikan sesuai dengan kebutuhan tubuh normal oleh sel beta dalam dua fase, sehingga sekresinya berbentuk biphasic. Seperti dikemukakan, sekresi insulin normal yang biphasic ini akan terjadi setelah adanya rangsangan seperti glukosa yang berasal dari makanan atau minuman. Insulin yang dihasilkan ini, berfungsi mengatur regulasi glukosa darah agar selalu dalam batas-batas fisiologis, baik saat puasa maupun setelah mendapat beban. Dengan demikian, kedua fase sekresi insulin yang berlangsung secara sinkron tersebut, menjaga kadar glukosa darah selalu dalam batas-batas normal, sebagai cerminan metabolisme glukosa yang fisiologis.
Sekresi fase 1 (acute insulin secretion responce = AIR) adalah sekresi insulin yang terjadi segera setelah ada rangsangan terhadap sel beta, muncul cepat dan berakhir juga cepat. Sekresi fase 1 (AIR) biasanya mempunyai puncak yang relatif tinggi, karena hal itu memang diperlukan untuk mengantisipasi kadar glukosa darah yang biasanya meningkat tajam, segera setelah makan. Kinerja AIR yang cepat dan adekuat ini sangat penting bagi regulasi glukosa yang normal karena pasa gilirannya berkontribusi besar dalam pengendalian kadar glukosa darah postprandial. Dengan demikian, kehadiran AIR yang normal diperlukan untuk mempertahankan berlangsungnya proses metabolisme glukosa secara fisiologis. AIR yang berlangsung normal, bermanfaat dalam mencegah terjadinya hiperglikemia akut setelah makan atau lonjakan glukosa darah postprandial (postprandial spike) dengan segala akibat yang ditimbulkannya termasuk hiperinsulinemia kompensatif.
Selanjutnya, setelah sekresi fase 1 berakhir, muncul sekresi fase 2 (sustained phase, latent phase), dimana sekresi insulin kembali meningkat secara perlahan dan bertahan dalam waktu relatif lebih lama. Setelah berakhirnya fase 1, tugas pengaturan glukosa darah selanjutnya diambil alih oleh sekresi fase 2. Sekresi insulin fase 2 yang berlangsung relatif lebih lama, seberapa tinggi puncaknya (secara kuantitatif) akan ditentukan oleh seberapa besar kadar glukosa darah di akhir fase 1, disamping faktor resistensi insulin. Jadi, terjadi semacam mekanisme penyesuaian dari sekresi fase 2 terhadap kinerja fase 1 sebelumnya. Apabila sekresi fase 1 tidak adekuat, terjadi mekanisme kompensasi dalam bentuk peningkatan sekresi insulin pada fase 2. Peningkatan produksi insulin tersebut pada hakikatnya dimaksudkan memenuhi kebutuhan tubuh agar kadar glukosa darah (postprandial) tetap dalam batas batas normal. Dalam prospektif perjalanan penyakit, fase 2 sekresi insulin akan banyak dipengaruhi oleh fase 1. Pada gambar dibawah ini diperlihatkan dinamika sekresi insulin pada keadaan normal, Toleransi Glukosa Terganggu (Impaired Glucose Tolerance = IGT), dan Diabetes Melitus Tipe 2.
Biasanya, dengan kinerja fase 1 yang normal, disertai pula oleh aksi insulin yang juga normal di jaringan (tanpa resistensi insulin), sekresi fase 2 juga akan berlangsung normal. Dengan demikian tidak dibutuhkan tambahan ( ekstra) sintesis maupun sekresi insulin pada fase 2 diatas normal untuk dapat mempertahankan keadaan normoglikemia. Ini adalah keadaan fisiologis yang memang ideal karena tanpa peninggian kadar glukosa darah yang dapat memberikan dampak glucotoxicity, juga tanpa hiperinsulinemia dengan berbagai dampak negatifnya.
Aksi Hormon Insulin
Insulin mempunyai fungsi penting pada berbagai proses metabolisme dalam tubuh terutama metabolisme karbohidrat. Hormon ini sangat krusial perannya dalam proses utilisasi glukosa oleh hampir seluruh jaringan tubuh, terutama pada otot, lemak, dan hepar. Pada jaringan perifer seperti jaringan otot dan lemak, insulin berikatan dengan sejenis reseptor (insulin receptor substrate = IRS) yang terdapat pada membran sel tersebut. Reseptor adalah molekul pengenal spesifik dari sel tempat hormon berikatan sebelum memulai efek biologisnya. Reseptor dapat ditemukan pada permukaan (membran plasma) ataupun intraseluler. Interaksi hormon dengan reseptor permukaan sel akan memberikan sinyal pembentukan senyawa. Reseptor insulin berupa heterotetramer (α2β2) yang mana terikat lewat ikatan disulfida yang multipel. Reseptor insulin merupakan reseptor tirosin kinase. Reseptor insulin memediasi aktivitasnya dengan memfosforilasi tirosin pada protein di dalam sel. Protein substrat yang difosforilasi oleh reseptor insulin termasuk protein yang disebut IRS-1 atau Insulin Receptor Substrate 1. Terfosforilasinya ikatan IRS-1 akan meningkatkan afinitas molekul transporter glukosa di membran luar jaringan yang responsif terhadap insulin seperti sel otot dan jaringan lemak, sehingga meningkatkan masuknya glukosa ke dalam sel.
Ikatan antara insulin dan reseptor akan menghasilkan semacam sinyal yang berguna bagi proses regulasi atau metabolisme glukosa didalam sel otot dan lemak, meskipun mekanisme kerja yang sesungguhnya belum begitu jelas. Setelah berikatan, transduksi sinyal berperan dalam meningkatkan kuantitas GLUT-4 (glucose transporter-4) dan selanjutnya juga pada mendorong penempatannya pada membran sel. Proses sintesis dan translokasi GLUT-4 inilah yang bekerja memasukkan glukosa dari ekstra ke intrasel untuk selanjutnya mengalami metabolism . Untuk mendapatkan proses metabolisme glukosa normal, selain diperlukan mekanisme serta dinamika sekresi yang normal, dibutuhkan pula aksi insulin yang berlangsung normal. Rendahnya sensitivitas atau tingginya resistensi jaringan tubuh terhadap insulin merupakan salah satu faktor etiologi terjadinya diabetes, khususnya diabetes tipe 2.
Baik atau buruknya regulasi glukosa darah tidak hanya berkaitan dengan metabolisme glukosa di jaringan perifer, tapi juga di jaringan hepar dimana GLUT-2 berfungsi sebagai kendaraan pengangkut glukosa melewati membrana sel kedalam sel. Dalam hal inilah jaringan hepar ikut berperan dalam mengatur homeostasis glukosa tubuh. Peninggian kadar glukosa darah puasa, lebih ditentukan oleh peningkatan produksi glukosa secara endogen yang berasal dari proses glukoneogenesis dan glikogenolisis di jaringan hepar. Kedua proses ini berlangsung secara normal pada orang sehat karena dikontrol oleh hormon insulin. Manakala jaringan ( hepar ) resisten terhadap insulin, maka efek inhibisi hormon tersebut terhadap mekanisme produksi glukosa endogen secara berlebihan menjadi tidak lagi optimal. Semakin tinggi tingkat resistensi insulin, semakin rendah kemampuan inhibisinya terhadap proses glikogenolisis dan glukoneogenesis, dan semakin tinggi tingkat produksi glukosa dari hepar.
Efek Metabolisme dari Insulin
Efek insulin pada glukosa
Gangguan, baik dari produksi maupun aksi insulin, menyebabkan gangguan pada metabolisme glukosa, dengan berbagai dampak yang ditimbulkannya. Pada dasarnya ini bermula dari hambatan dalam utilisasi glukosa yang kemudian diikuti oleh peningkatan kadar glukosa darah. Secara klinis, gangguan tersebut dikenal sebagai gejala diabetes melitus. Pada diabetes melitus tipe 2 (DMT2), yakni jenis diabetes yang paling sering ditemukan, gangguan metabolisme glukosa disebabkan oleh dua faktor utama yakni tidak adekuatnya sekresi insulin (defisiensi insulin) dan kurang sensitifnya jaringan tubuh terhadap insulin (resistensi insulin), disertai oleh faktor lingkungan ( environment ). Sedangkan pada diabetes tipe 1 (DMT1), gangguan tersebut murni disebabkan defisiensi insulin secara absolut.
Gangguan metabolisme glukosa yang terjadi, diawali oleh kelainan pada dinamika sekresi insulin berupa gangguan pada fase 1 sekresi insulin yang tidak sesuai kebutuhan (inadekuat). Defisiensi insulin ini secara langsung menimbulkan dampak buruk terhadap homeostasis glukosa darah. Yang pertama terjadi adalah hiperglikemia akut pascaprandial (HAP) yakni peningkatan kadar glukosa darah segera (10-30 menit) setelah beban glukosa (makan atau minum).
Kelainan berupa disfungsi sel beta dan resistensi insulin merupakan faktor etiologi yang bersifat bawaan (genetik). Secara klinis, perjalanan penyakit ini bersifat progressif dan cenderung melibatkan pula gangguan metabolisme lemak ataupun protein. Peningkatan kadar glukosa darah oleh karena utilisasi yang tidak berlangsung sempurna pada gilirannya secara klinis sering memunculkan abnormalitas dari kadar lipid darah. Untuk mendapatkan kadar glukosa yang normal dalam darah diperlukan obat-obatan yang dapat merangsang sel beta untuk peningkatan sekresi insulin ( insulin secretagogue ) atau bila diperlukan secara substitusi insulin, disamping obat-obatan yang berkhasiat menurunkan resistensi insulin ( insulin sensitizer ).
Tidak adekuatnya fase 1, yang kemudian diikuti peningkatan kinerja fase 2 sekresi insulin, pada tahap awal belum akan menimbulkan gangguan terhadap kadar glukosa darah. Secara klinis, barulah pada tahap dekompensasi, dapat terdeteksi keadaan yang dinamakan Toleransi Glukosa Terganggu yang disebut juga sebagai prediabetic state. Pada tahap ini mekanisme kompensasi sudah mulai tidak adekuat lagi, tubuh mengalami defisiensi yang mungkin secara relatif, terjadi peningkatan kadar glukosa darah postprandial. Pada toleransi glukosa terganggu (TGT) didapatkan kadar glukosa darah postprandial, atau setelah diberi beban larutan 75 g glukosa dengan Test Toleransi Glukosa Oral ( TTGO ), berkisar diantara 140-200 mg/dl. Juga dinamakan sebagai prediabetes, bila kadar glukosa darah puasa antara 100 – 126 mg/dl, yang disebut juga sebagai Glukosa Darah Puasa Terganggu ( GDPT ).
Keadaan hiperglikemia yang terjadi, baik secara kronis pada tahap diabetes, atau hiperglikemia akut postprandial yang terjadi ber-ulangkali setiap hari sejak tahap TGT, memberi dampak buruk terhadap jaringan yang secara jangka panjang menimbulkan komplikasi kronis dari diabetes.Tingginya kadar glukosa darah (glucotoxicity) yang diikuti pula oleh dislipidemia (lipotoxicity) bertanggung jawab terhadap kerusakan jaringan baik secara langsung melalui stres oksidatif, dan proses glikosilasi yang meluas.
Resistensi insulin mulai menonjol peranannya semenjak perubahan atau konversi fase TGT menjadi DMT2. Dikatakan bahwa pada saat tersebut faktor resistensi insulin mulai dominan sebagai penyebab hiperglikemia maupun berbagai kerusakan jaringan. Ini terlihat dari kenyataan bahwa pada tahap awal DMT2, meskipun dengan kadar insulin serum yang cukup tinggi, namun hiperglikemia masih dapat terjadi. Kerusakan jaringan yang terjadi, terutama mikrovaskular, meningkat secara tajam pada tahap diabetes, sedangkan gangguan makrovaskular telah muncul semenjak prediabetes. Semakin tingginya tingkat resistensi insulin dapat terlihat pula dari peningkatan kadar glukosa darah puasa maupun postprandial. Sejalan dengan itu, pada hepar semakin tinggi tingkat resistensi insulin, semakin rendah kemampuan inhibisinya terhadap proses glikogenolisis dan glukoneogenesis, menyebabkan semakin tinggi pula tingkat produksi glukosa dari hepar.
Jadi, dapat disimpulkan perjalanan penyakit DMT2, pada awalnya ditentukan oleh kinerja fase 1 yang kemudian memberi dampak negatif terhadap kinerja fase 2, dan berakibat langsung terhadap peningkatan kadar glukosa darah (hiperglikemia). Hiperglikemia terjadi tidak hanya disebabkan oleh gangguan sekresi insulin (defisiensi insulin), tapi pada saat bersamaan juga oleh rendahnya respons jaringan tubuh terhadap insulin (resistensi insulin). Gangguan atau pengaruh lingkungan seperti gaya hidup atau obesitas akan mempercepat progresivitas perjalanan penyakit. Gangguan metabolisme glukosa akan berlanjut pada gangguan metabolisme lemak dan protein serta proses kerusakan berbagai jaringan tubuh. Rangkaian kelainan yang dilatarbelakangi oleh resistensi insulin, selain daripada intoleransi terhadap glukosa beserta berbagai akibatnya, sering menimbulkan kumpulan gejala yang dinamakan sindroma metabolik.
Efek insulin pada metabolisme lemak
Insulin mempunyai berbagai efek yang dapat menyebabkan timbulnya penyimpanan lemak didalam jaringan lemak. Pertama, insulin meningkatkan pemakaian glukosa oleh sebagian besar jaringan tubuh yang secara otomatis akan mengurangi pemakaian lemak. Akan tetapi, insulin juga meningkatkan pembentukan asam lemak. Hal itu terjadi jika karbohidrat lebih banyak dicerna daripada energi spontan yang digunakan jadi mempersiapkan zat untuk sintesis lemak.
Insulin juga merupakan inhibitor atau penghambat kuat proses lipolisis (penghambatan pengeluaran lemak ke aliran darah) dalam hati serta jaringan adiposa dan dengan demikian memiliki efek anabolik tak langsung. Hal ini sebagian disebabkan oleh kemampuan insulin untuk menurunkan kadar cAMP (yang dalam jaringan ini ditingkatkan oleh homon lipolitik gluokagon dan epinefrin) tetapi juga oleh kenyataan bahwa insulin juga menghambat aktivitas enzim lipase yang peka terhadap kerja hormon Inhibisi ini agaknya disebabkan oleh akitasi fosfatase yang melakukan reaksi defosforilasi dan dengan demikian meniadakan keaktifan enzim lipase atau enzim protein kinase yang bergantung pada cAMP. Karena itu, insulin menurunkan kadar asam emak bebas yang berbeda. Hal ini turut menghasilkan kerja insulin terhadap metabolisme karbohidrat, mengingat asam lemak menghambat glikolisis pada beberapa tahap dan menstimulasi glukoneogeneis. Jadi, pengaturan metabolic tidak dapat dibicarakan dalam konteks suatu hormon atau metabolit yang tunggal. Proses pengaturan merupakan proses yang kompleks dimana aliran suatu lintasan tertentu terjadi akibat interaksi sejumlah hormon dan metabolit.
Pada penderita defisiensi insulin akan terjadi peningkatan aktifitas enzim lipase. Pada keadaan normal insulin menghambat aktifitas enzim lipase, hal ini dikarenakan insulin bertugas untuk menghambat aktivitas enzim lipase dimana enzim ini menyebabkan hidrolisis trigliserida yang telah disimpan dalam sel-sel lemak oleh karena itu, pelepasan asam lemak dari jaringan adiposa ke dalam sirkulasi darah akan terhambat. Pada keadaan defisiensi insulin maka akan terjadi penghambatan aktifitas enzim lipase yang mengakibatkan penggalakan lipolisis dan peningkatan konsentrasi asam lemak bebas dalam plasma serta hati. Kadar glukagon juga meningkat pada pasien ini dan hal ini menggiatkan pelepasan asam lemak bebas. Glukagon melawan sebagian besar kerja insulin, dan keadaan metabolisme pada diri seorang penderita diabetes merupakan pencerminan kadar relatif glukagon dan insulin. Sebagian asam lemak bebas dimetabolisasi menjadi asetil KoA (pembalikan lipogenesis). Dan kemudian menjadi Carbondioksida dan Hidrogen lewat siklus asam sitrat. Pada pasien defisiensi insulin, kapasitas proses ini dengan cepat akan dilampaui dan asetil KoA akan diubah menjadi asetoasetil KoA serta kemudian Insulin tampaknya mempengaruhi pembentukan atau klirens VLDL serta LDL mengikat kadar partikel ini dan sebagai konsekuensinya juga kadar kolesterol,sering mengalami kenaikan pada penderita diabetes yang tidak terkontrol. Percepatan proses ateroskleosis yang menjadi permasalahan serius pada banyak penderita diabetes,ditimbulkan oleh cacat metabolik ini.
Efek metabolisme insulin pada protein
Insulin menyebabkan pengangkutan secara aktif sebagian besar asam amino dari darah kedalam sel, hal ini dapat dilakukan oleh insulin bersama dengan hormon pertumbuhan, akan tetapi, asam amino yang dipengaruhi bukanlah asam amino yang sama. Insulin juga meningkatkan translasi mRNA pada ribosom sehingga terbentuk protein baru dengan jalan “menyalakan” mesin ribosom sehingga meningkatkan kecepatan transkripsi DNA dalam inti sel akibatnya jumlah RNA naik sehingga sintesis protein akan terjadi. Bila tidak ada insulin, maka ribosom akan berhenti bekerja. Insulin juga menghambat proses katabolisme protein, jadi mengurangi kecepatan pelepasan asam amino dari sel, khususnya dari sel-sel otot. Hal ini akibat dari beberapa kemampuan insulin untuk mengurangi pemacahan insulin yang normal lisosom sel. Di dalam hati, insulin menekan kecepatan glukoneogenesis. Hal ini terjadi dengan cara mengurangi aktivitas enzim yang dapat meningkatkan glukogenesis. Oleh karena itu bahan yang terbanyak digunakan untuk sintesis glukosa melalui prose glukoneogenesis adalah asam amino dalam plasma, maka proses penekanan glukogenesis akan menghemat pemakaian asam amino dari cadangan protein dalam tubuh.
Jika terjadi defisiensi atau kekurangan insulin, maka akan terjai hal yang sebaliknya. Tidak adanya insulin menyebabkan berkurangnya protein dan peningkatan asam amino plasma. Bila tidak ada insulin maka seluruh proses penyimpanan protein menjadi terhenti sama sekali. Proses katabolisme atau pemecahan protein akan meningkat, sintesis protein berhenti, dan banyak sekali asam amino ditimbun dalam darah. Konsentrasi asam amino dalam darah sangat meningkat dan sebagian besar asam amino yang berlebihan akan langsung dipergunakan sumber energi atau sebagian bahan yang akan hidup dalam proses glukoneogenesis. Pemecahan asam amino ini juga meningkatkan eskresi ureum dalam urine. Sampah protein yang dihasilkan merupakan salah satu efek yang serius pada penyakit diabetes mellitus yang parah. Hal ini dapat menimbulkan kelemahan yang hebat dan juga terganggunya fungsi organ-organ.
Hal-Hal Yang Mempengaruhi Sekresin Insulin
Perangsangan sekresi insulin oleh glukosa darah
- Konsentrasi glukosa dalam darah meningkat menyebabkan sekresi insulin meningkat. Dalam waktu 3 sampai 5 menit sesudah terjadi peningkatan segera kadar glukosa darah, insulin meningkat sampai hampir 10 kali lipat. Keadaan ini disebabkan oleh pengeluaran insulin yang sudah terbentuk lebih dahulu oleh sel beta pulau langerhans pancreas. Akan tetapi, kecepatan sekresi awal yang tinggi ini tidak dapat dipertahankan, sebaliknya, dalam waktu 5 sampai 10 menit kemudian kecepatan sekresi insulin akan berkurang sampai kira-kira setengah dari kadar normal. Kira-kira 15 menit kemudian, sekresi insulin meningkat untuk kedua kalinya, sehingga dalam waktu 2 sampai 3 jam akan mencapai gambaran seperti dataran yang baru, biasanya pada saat ini kecepatan sekresinya bahkan lebih besar daripada kecepatan sekresi pada tahap awal. Sekresi ini disebabkan oleh adanya tambahan pelepasan insulin yang sudah lebih dahulu terbentuk dan oleh adanya aktivasi system enzim yang mensintesis dan melepaskan insulin baru dari sel.
- Naiknya sekresi insulin akibat stimulus glukosa menyebabkan meningkatnya kecepatan dan sekresi secara dramatis. Selanjutnya, penghentian sekresi insulin hampir sama cepatnya, terjadi dalam waktu 3 sampai 5 menit setelah pengurangan konsentrasi glukosa kembali ke kadar puasa.
- Peningkatan glukosa darah meningkatkan sekresi insulin dan insulin selanjutnya meningkatkan transport glukosa ke dalam hati, otot, dan sel lain, sehingga mengurangi konsentrasi glukosa darah kembali ke nilai normal.
- Pemberian asam amino sewaktu tidak ada peningkatan kadar glukosa darah maka peningkatan sekresi insulin sedikit saja. Namun bila pemberian insulin pada saat terjadi peningkatan glukosa darah maka sekresi insulin yang diinduksi oleh glukosa dapat berlipat ganda saat kelebihan asam amino. Jadi, asam amino sangat memperkuat rangsangan glukosa terhadap sekresi insulin. Tampaknya perangsangan sekresi insulin oleh asam amino merupakan respons yang sangat bermakna sebab insulin sendiri sebaliknya meningkatkan pengangkutan asam amino ke dalam sel jaringan demikian juga meningkatkan pembentukan protein intraselular. Sehingga hal ini menyebabkan insulin sangat berguna untuk pemakaian asam amino yang berlebihan.
- Campuran gastrin, sekretin, kolesistokinin, dan peptide penghambat asam lambung ( hormone terkuat dari seluruh hormone kelenjar pencernaan ) akan meningkatkan sekresi insulin ( peningkatan “antisipasi” insulin dalam darah disebabkan persiapan agar glukosa dan asam amino dapat diabsorbsi dari makanan tersebut ). Hormone ini dilepaskan sesudah seseorang makan.
- Selanjutnya hormon gastrointestinal ini akan menyebabkan antisipasi insulin dalam darah yang merupakan suatu persiapan agar glukosa dan asam amino dapat diabsorbsi. Hormon ini bekerja sama dengan asam amino yaitu meningkatkan sensitivitas respon insulin untuk meningkatkan glukosa darah, yang hampir mengdakan kecepatan sekresi insulin bersamaan dengan naiknya glukosa darah.
- Glukagon, GH, kortisol, progesteron, dan estrogen. Pemanjangan sekresi salah satu jenis hormone ini mengakibatkan sel beta pulau langerhans pancreas menjadi lelah dan akibatnya timbullah diabetes. Memang, diabetes sering terjadi pada orang yang menggunakan dosis farmasi tinggi dari beberapa hormone ini.
- Perangsangan saraf parasimpatis atau saraf simpatis terhadap pancreas juga meningkatkan sekresi insulin.
Efek Kekurangan Insulin Bagi Tubuh
Difisiensi insulin (kekurangan insulin) atau reseptor insulin tidak berfungsi baik, dimana dapat mempengaruhi metabolisme tubuh yang berdampak terhadap system tubuh yaitu :
Efek pada Sistem endokrin
- Defisiensi insulin menyebabkan kegagalan dalam pemasukan nutrisi kejaringan sehingga swell-sel kekurangan glukosa yang menimbulkan Sel kekurangan glukosa untuk proses metabolisme dan penurunan penggunaan dan aktivitas glukosa dalam sel akan merangsang pusat lapar, Penurunan penggunaan protein dan glukosa oleh jaringan sehingga menyebabkan penurunan berat badan dan Pembongkaran lemak dan cadangan protein untuk memenuhi kebutuhan metabolisme proses ini menghasilkan benda-benda keton yang disebabkan hati yang tidak mampu menetralisir lemak. Penumpukan asam lemak ini akan mengiritasi memperoleh peningkatan sekresi asam lambung sehingga menimbulkan gangguan system ini berdampak terhadap gangguan kebutuhan nutrisi
- Peningkatan kadar glukosa darah akan mengakibatkan penumpukan sorbitol dan lemak pada tunika intima sehingga pembuluh darah mengalami penyempitan. Jika hal ini terjadi maka suplai O2 dan nutrisi akan berkurang kejaringan dan terjadilah infark pada jaringan yang dituju, apabila mengenai pembuluh darah perifer akan menimbulkan efek penurunan sensasi sehingga akan terjadi gangrene ekstremitas bila terjadi trauma. Dan jika terjadi pada arteri jantung akan menyebabkan angina pectoris dan akut miokard imfark.
- Defisiensi insulin menyebabkan kegagalan dalam pemasukan glukosa kejaringan sehingga sel-sel kekurangan glukosa. Proses kekurangan glukosa intra sel menimbulkan : Peningkatan penggunan protein dan glukogen oleh jaringan sehingga menyebabkan penurunan berat badan, Pembongkaran lemak dan cadangan protein untuk memenuhi kebutuhan metabolisme. Hal ini akan diperberat oleh peningkatan sekresi asam lambung sehingga menimbulkan perasaan mual, muntah dan Peningkatan transport glukosa untuk proses metabolisme. Penurunan penggunaan dan aktivitas glukosa dalam sel akan merangsang pusat makan dibagian lateral hypothalamus, sehingga timbul peningkatan perasaan lapar ( poliphagi )
- Kekurangan pemasukan glukosa kedalam sel menyebabkan peningkatan volume extra sel sehingga terjadi peningkatan osmolalitas sel yang akan merangsang hypothalamus untuk mengsekresikan ADH dan merangsang pusat haus di bagian lateral. Pada fase ini klien akan merasakan haus dan penurunan produksi urine sehingga volume cairan extra sel bertambah. Peningkatan volume cairan akan menyebabkan konsentrasi extra sel menurun sehingga cairan intra sel menurun. Penurunan volume intra sel merangsang volume reseptor di Hipothalamus untuk menekan sekresi ADH sehingga terjadi peningkatan kadar gula darah melebihi ambang ginjal. Diuresis osmotic akan mempercepat pengisian vesika urinaria sehingga merangsang keinginan berkemih (poliuri) dan kondisi ini bertambah pada mlam hari karena terjadi vasokonstriksi akibat penurunan suhu sehingga timbul nokturi. Selain itu gangguan system perkemihan juga terjadi akibat adanya kerusakan ginjal ( netropati ) hal ini disebabkan adanya penurunan perfusi kedaerah ginjal. Gangguan ini dapat berdampak pada Gangguan keseimbangan cairan dan elektrolit, Gangguan pola eliminasi BAK dan Perubahan pola istirahat tidur
- Defisiensi insulin menghambat transportasi glukosa kesel-sel dalam jaringan tubuh yang menyebabkan sel kelaparan dan terjadi peningkatan glukosa dalam darah menyebabkan hambatan dalam perfusi ke jaringan yang mengakibatkan jaringan kurang mendapat Oksigen dan nutrisi.
- Penurunan transport glukosa ke sel dan penurunan Oksigen dan nutrisi ke sel menyebabkan sel kekurangan bahan untuk metabolisme sehingga energi yang dihasilkan berkurang yang berdampak timbulnya kelemahan. Selain itu defisiensi insulin menyebabkan penurunan jumlah sintesa glikogen dalam otot serta peningkatan metabolisme protein yang berguna untuk pertumbuhan sel-sel tubuh.
- Defisiensi insulin dapat berdampak pada integritas kulit yang bisa disebabkan oleh neuropati diabetes dan angiopati diabetes , angiopati diabetes akan menyebabkan peurunan sensasi sehingga pengontrolan terhadap trauma mekanis, termis dan kimia menurun, hal ini akan memudahkan terkena luka yang mengancam keutuhan kulit sedangkan teori yang lain mendasari kerusakan kulit adanya kerusakan membrane basalis yang terjadi akibat adanya penumpukan endapan lipoprotein sehingga menyebabkan kebocoran protein dan butir-butir darah.Pertahanan dan perfusi jaringan menurun dengan akibat kulit mudah infeksi, luka sukar sembuh, mudah selulit gangrene. Dampaknya akan menyebabkan Gangguan rasa nyaman nyeri dan gatal dan Gangguan integritas kulit
- Defisiensi insulin menumbulkan hambatan, pemasukan glukosa kedalam sel termasuk sel-sel syaraf, sehingga mengganggu proses metabolisme sel syaraf. Akibat kekurangan glukosa sebagai bahan metabolisme maka sel akan menggunakan cadangan protein. Hal ini mengakibatkan sel kekurangan protein, akan mempengaruhi pembentukan myelin yang berfungsi untuk menghantarkan impuls pada akson, selain itu akan menyebabkan kerusakan akson tidak dapat mengantarkan impuls dengan sempurna selain kekurangan protein, kegagalan metabolisme sel saraf dapat menyebabkan hambatan dalam konduksi saraf dan polarisasi membrane akibat penurunan ATP. Perubahan-perubahan diatas menyebabkan gangguan polineropatik perifer yang ditandai kurangnya sensasi apda ujung-ujung ekstremitas bawah.
- Defisiensi insulin dapat menyebabkan terjadinya impotensi pada laki-laki dan penurunan libido pada wanita. Hal ini disebabkan oleh adanya hambatan pengikatan ekstra diar pada gugus protein akibat kegagalan metabolisme protein. Pada wanita sering juga terdapat keluhan keputihan disebabkan infeksi kandida. Dampaknya akan berpengaruh pada gangguan pemenuhan kebutuhan seksual
- Hiperglikemi akan mengakibatkan penumpukan kadar glukosa pada sel dan jaringan tertentu yang dapat mentranspor glikosa tanpa memerlukan insulin, glukosa yang berlebihan ini tidak bermetabolisme habis secara normal melalui glukolisis tetapi sebagian dengan pertolongan enzim aldose reduktase atau diubah menjadi sorbitol. Sorbitol akan bertumpuk dalam jaringan / sel tersebut, sehingga menyebabkan kerusakan dan perubahan fungsi. Teori ini mendasari kelainan diabetes mellitus pada mata dengan adanya retinopati, selain itu pada penderita DM bisa ditemukan adanya katarak, hal ini disebabkan pengendapan lipoprotein pada lensa mata.
DAFTAR PUSTAKA
- Hafiz, Soewoto. 2009. Hormon-hormon yang Berperan dalam Proses Metabolisme. Dep. Biokimia dan Biologi Molekuler F.K.U.I
- Ferrannini E, 1998. Insulin resistance versus insulin deficiency in non insulin dependent diabetes mellitus: Problems and prospects. Endocrine Reviews 19: 477-90.
- Gerich JE, 1998. The genetic basis of type 2 diabetes mellitus: impaired insulin secretion versus impaired insulin sensitivity. Endocrine Reviews 19: 491-503.
- Girard J, 1995. NIDDM and glucose transport in cells. In ( Assan, R, ed ) NIDDM and glucose transport in cells. Molecular Endocrinology and Development CNRS Meudon, France: 6 – 16.
- Kramer W, 1995. The molecular interaction of sulphonylureas. DRCP 28: 67 – 80
- Lehninger, A.L. 1982. Dasar Dasar Biokimia. Erlangga. Jakarta.
- Manaf, Asman. 2006. Insulin: Mekanisme Sekresi dan Aspek Metabolisme. Buku Ajar Ilmu Penyakit Dalam. Jakarta: Pusat Penerbitan Departemen Ilmu Penyakit Dalam FKUI. Hal 1890,
- Nielsen MF, Nyholm B, Caumo A, Chandramouli V, Schumann WC, Cobelli C, et al, 2000. Prandial glucose effectiveness and fasting gluconeogenesis in insulin-resistant first-degree relatives of patients with type 2 diabetes. Diabetes 49: 2135-41.
- Prato SD, 2002. Loss of early insulin secretion leads to postprandial hyperglycaemia. Diabetologia 29: 47-53.
- Suryohudoyo P, 2000. Ilmu kedokteran molekuler. Ed I, Jakarta: Perpustakaan Nasional, hlm 48-58.
- Suzuki H, Fukushima M, Usami M, Ikeda M, Taniguchi A, Nakai Y, et al,2003.Factors responsible for development from normal glocose tolerance to isolated postchallenge hyperglycemia. Diabetes Care 26: 1211-5.
- Tjokroprawiro A, 1999. Diabetes mellitus and syndrome 32 (A step forward to era of globalisation–2003). JSPS-DNC symposium, Surabaya: 1-6.
- Ward WD, 1984. Pathophysiology of insulin secretion in non insulin dependent diabetes mellitus. Diabetes Care 7 : 491 - 502
- Weyer C, Bogardus C, Mort DM, Tataranni PA, Pratley RE, 2000. Insulin resistance and insulin secretory dysfunction are independent predictors of worsening of glucose tolerance during each stage of type 2 diabetes development. Diabetes Care 24: 89-94.