PENGOBATAN PENYAKIT JANTUNG KRONIS PERIOPERATIF
- Penggunaan obat-obat kardiovaskuler biasanya diperlukan pada 2 keadaan; Pertama : pengobatan kardiovaskuler untuk jangka panjang (biasanya dalam sediaan peroral) sebelum pembedahan. Kedua : pengobatan segera (biasanya bentuk sediaan intravena) pada periode perioperatif dalam keadaan akut di Coronary Care Unit, intraoperatif dan/atau pasca operatif.
- Keperawatan perioperatif adalah istilah yang digunakan untuk menggambarkan keragaman fungsi keperawatan yang berkaitan dengan pengalaman pembedahan pasien. Pengertian Kata perioperatif adalah suatu istilah gabungan yang mencangkup 3 fase pengalaman pembedahan yaitu Praoperatif, Intraoperatif dan Pascaoperatif
- Fase praoperatif dimulai ketika keputusan untuk intervensi dibuat dan berakhir ketika pasien dikirim ke meja operasi. Fase intraoperatif dimulai ketika pasien masuk atau pindah ke bagian atau departemen bedah dan berakhir pada saat pasien dipindahkan ke ruang pemulihan. Fase postoperatif dimulai dengan masuknya pasien ke ruang pemulihan dan berakhir dengan evaluasi tindak lanjut pada tatanan klinik atau dirumah.
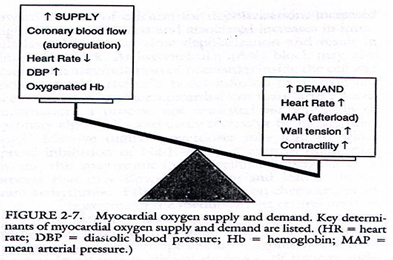
- Pemahaman yang rasional dalam pemberian medikamentosa kardiovaskuler kronis untuk pengobatan hipertensi dan/atau penyakit jantung iskemik didasarkan pada keseimbangan suplai dan kebutuhan oksigen miokard. Kebutuhan oksigen miokard ditentukan oleh peningkatan laju jantung, peningkatan afterload (MAP), peningkatan tekanan dinding ventrikel (resultante pembebanan volume terhadap ventrikel kiri) dan peningkatan kontraktilitas. Suplai oksigen miokard ditentukan oleh aliran darah koroner (efek metabolik setempat, autoregulasi, dan sifat pembuluh darah koroner), penurunan laju jantung (memberikan waktu lebih lama untuk perfusii koroner selama diastolik), peningkatan tekanan darah diastolik (memberikan peningkatan tekanan perfusi koroner menyeluruh), dan kapasitas angkut oksigen dari darah.
- Oleh karena laju jantung tampak pada kedua sisi, parameter tersebut makin jelas berpotensi menyebabkan atau mengurangi iskemik miokard saat munculnya lesi aliran terbatas pada arteri koronaria. Pada saat laju jantung meningkat, kebutuhan oksigen miokard meningkat dimana suplai menurun, berpotensi untuk terjadinya iskemik miokard.
- Jika terjadi penurunan laju jantung, secara umum kebutuhan oksigen miokard menurun dan waktu perfusi koroner meningkat, sehingga meningkatkan suplai oksigen ke miokard, terutama pada subendokardium ventrikel kiri dimana pada saat sistol tidak mendapat suplai darah koroner oleh karena tekanan pada pembuluh darah koroner intramiokard.
- Perubahan salah satu parameter kardiovaskuler sering kali merubah parameter yang lain. (contoh: penurunan laju jantung akan meningkatkan venous return, berpotensi meningkatkan volume dan tekanan dinding ventrikel). Oleh karena itu, pemahaman yang menyeluruh tentang keterkaitan di dalam sistem kardiovaskuler sangat penting untuk penatalaksanaan penyakit jantung iskemik yang rasional, dan memungkinkan kita untuk dapat memprediksi berbagai kemungkinan akibat dari manipulasi kardiovaskuler yang kita berikan, sehingga dapat dipilih jenis obat yang diperlukan.
- Beberapa penyakit miokardial mungkin membutuhkan pengobatan untuk waktu yang lama, dan pada saat pasien tersebut memerlukan tindakan operasi non jantung, sering kali mereka masih menggunakan obat-obat oral yang cukup banyak. Beberapa penyakit kardiovaskuler yang membutuhkan pengobatan jangka panjang seperti gagal jantung kongestif, hipertensi dan iskemia miokard. Penyakit penyerta yang lain seperti gagal ginjal kronik dan diabetes melitus biasanya juga mendapat terapi.
- Pengobatan jangka panjang terhadap penyakit kardiovaskuler yang paling sering ditemui pada saat preoperasi adalah digitalis, diuretik, vasodilator koroner termasuk nitrat, antagonis beta-AR dan antagonis saluran kalsium. Mekanisme aksi dari obat-obat tersebut beserta interaksi (jika ada) dengan obat-obat anestesi akan kita bahas pada tinjauan pustaka ini.
DIGITALIS
- Tanaman obat yang mengandung glikosida jantung sudah dikenal sejak zaman Mesir kuno. Bangsa Romawi menggunakannya sebagai diuretik, penguat jantung, perangsang muntah dan racun tikus. Dalam dunia kedokteran moderen, kegunaan digitalis sebagai obat telah dikukuhkan oleh William Withering (1875) dalam risalahnya yang berjudul An Account of the Foxglove and Some of Its Medical Uses: with Practical Remarks on Dropsy and Other Diseases.
- Sifat farmakodinamik utama digitalis adalah inotropik positif, yaitu meningkatkan kekuatan kontraksi miokardium. Pada pasien yang mengalami gangguan fungsi sistolik, efek inotropik positif ini akan menyebabkan peningkatan curah jantung sehingga tekanan vena berkurang, ukuran jantung mengecil, dan reflek takikardia yang merupakan kompensasi jantung diperlambat.
- Tekanan vena yang berkurang akan mengurangi gejala bendungan, sedangkan sirkulasi yang membaik, termasuk ke ginjal, akan meningkatkan diuresis dan hilangnya udem. Digitalis juga menyebabkan perlambatan denyut ventrikel pada fibrilasi dan fluter atrium, dan pada kadar toksik menimbulkan disritmia. Jadi efektivitas digitalis pada gagal jantung kongestif timbul karena kerja langsungnya dalam meningkatkan kontraksi miokardium.
- Digitalis juga bekerja langsung pada otot polos pembuluh darah, selain itu efeknya pada jaringan saraf mempengaruhi secara tidak langsung aktivitas mekanik dan listrik jantung serta resistensi dan daya tampung pembuluh darah. Akhirnya, perubahan dalam sirkulasi akibat digitalis sering diikuti oleh perubahan reflek pada aktivitas otonom dan keseimbangan hormonal yang secara tidak langsung berpengaruh baik terhadap fungsi kardiovaskuler. Efek langsung maupun tak langsung ini, keduanya mempengaruhi sistem mekanik (kontraktilitas) dan listrik jantung.
- Mekanisme meningkatnya kontraktilitas otot jantung oleh digitalis sangat kompleks. Besarnya efek ini sesuai dengan besarnya dosis (dose-dependent positive inotropic effect). Efek ini berlaku untuk otot atrium dan ventrikel, dan secara kualitatif sama untuk otot jantung yang normal maupun yang gagal.
- Mekanisme kerja efek inotropik positif digitalis didasarkan atas 2 hal, yaitu :
- (1) penghambatan enzim Na+, K+ adenosin trifosfatase (Na+, K+-ATPase) yang terikat di membran sel miokard (sarkolema) dan berperan dalam mekanisme pompa Na+; dan
- (2) peningkatan arus masuk lambat (slow inward current) Ca+ ke intrasel pada potensial aksi.
- Pada fisiologi otot jantung terjadi pertukaran ion-ion di intrasel dan ekstrasel. Pertukaran ini terjadi karena perbedaan kadar ion-ion tersebut di dalam dan luar sel, misalnya pada pertukaran Ca++ intrasel dengan Na+ ekstrasel. Selain itu terjadi juga pertukaran ion melalui mekanisme pompa yang memerlukan energi karena keluar masuknya ion melawan kadar yang tinggi. Ini terjadi pada pertukaran Na+ dan K+ melalui suatu mekanisme pompa.
- Energi untuk pompa Na+ diperoleh dari hidrolisis ATP oleh enzim Na+, K+-ATPase, maka penghambatan enzim ini menyebabkan terhambatnya pertukaran K+ ekstrasel dengan Na+ intrasel dengan akibat meningginya kadar Na+ dan menurunnya K+ di dalam sel. Peningkatan Na+ intrasel ini menyebabkan pertukaran Ca++ intrasel dengan Na+ ekstrasel melalui sistem carrier Na+-Ca++ exchange terhambat dan Ca++ intrasel meningkat.
- Disamping itu, oleh sebab yang belum diketahui dengan jelas, peningkatan kadar Ca++ intrasel akan menyebabkan semakin banyaknya Ca++ yang masuk lewat slow channel. Ion Ca++ yang masuk kedalam sel menyebabkan penglepasan Ca++ tambahan dari depot intraseluler (sarkoplasmik retikulum). Peningkatan kadar Ca++ intrasel akan menyebabkan semakin banyak Ca++ yang terikat pada reseptornya di miofibril (troponin C) dan memperkuat kontraksi jantung.
- Tidak diragukan lagi bahwa berbagai efek digitalis terhadap aktivitas listrik dan mekanik jantung mamalia didasarkan atas pengaruhnya terhadap aktivitas saraf otonom dan sensitivitas jantung terhadap neurotransmitor saraf tersebut. Penurunan frekuensi sinus oleh digitalis (efek kronotropik negatif) pada gagal jantung sebagian besar disebabkan oleh peningkatan efek vagal dan sebagian lagi karena penurunan tonus simpatis secara refleks. Perubahan ini diikuti dengan perbaikan sirkulasi. Perubahan aktivitas otonom lainnya sangat kompleks dan belum dipahami benar.
- Efek tak langsung pada sistem saraf otonom terjadi pada kadar terapi dan kadar toksik. Pada kadar rendah efek parasimpatomimetik lebih menonjol. Peningkatan aktivitas vagus ini kelihatannya merupakan gabungan efek pada berbagai tempat di sistem saraf yaitu baroreseptor di arteri, nukleus vagus sentral, ganglion nodosum dan ganglion otonom. Karena persarafan kolinergik lebih banyak di atria, maka efek tak langsung ini lebih jelas di atria dan nodus AV daripada di serabut Purkinye. Selain itu ada bukti bahwa digitalis meningkatkan kepekaan nodus SA terhadap asetilkolin.
- Dapat dikatakan bahwa efek tak langsung digitalis yang terutama diperantarai oleh vagus, menyebabkan perubahan aktivitas nodus SA, atrium, dan nodus AV. Dalam kadar terapi, efek tak langsung terhadap fungsi sistem hantaran ventrikel dan otot ventrikel tidak berarti
Tabel Dosis, waktu timbulnya efek dan nasib digoksin dan digitoksin
Digoksin
|
Digitoksin
| |
Dosis digitalisasi (rata-rata)
Oral
IV
Dosis pemeliharaan per hari (rata-rata)
Oral
IV
Mula kerja
Oral
IV
Efek maksimal
Oral
IV
Absorpsi intestinal
Ikatan protein plasma
Waktu paruh disposisi
Jalur eliminasi
Siklus enterohepatik
Kadar terapi (plasma)
|
0,75 – 1,5 mg
0,5 – 1,0 mg
0,125 – 0,5 mg
0,25 mg
1,5 – 6 jam
5 – 30 menit
4 – 6 jam
1,5 – 3 jam
40 – 90% (75%)
25%
1,6 hari
ginjal
sedikit
0,5 – 2,0 ng/ml
|
0,8 – 1,2 mg
0,8 – 1,2 mg
0,05 – 0,2 mg
0,1 mg
3 – 6 jam
30 – 120 menit
6 – 12 jam
4 – 6 jam
90 – 100%
95%
4 – 7 hari
hati
banyak
10 – 35 ng/ml
|
- Salah satu efek samping digitalis yang paling mengancam jiwa adalah terjadinya aritmia. Hal tersebut terlihat ironis, disatu sisi digitalis digunakan untuk terapi atrial fibrilasi dengan cara memperlambat respon ventrikel terhadap cepatnya laju atrium, disisi lain peningkatan konsentrasi kalsium intraseluler memperantarai peningkatan inotropik digitalis yang akan menyebabkan aritmia.
- Efek samping langsung disebabkan oleh hambatan terhadap pompa sodium oleh inhibisi Na-K-ATPase (termasuk perubahan dalam depolarisasi membran konduksi, automatisitas dan eksitabilitas), keterlambatan afterpotential dan aftercontraction mekanik oleh digitalis yang menyebabkan aritmia ventrikuler. Oleh karena depolarisasi atrium tergantung pada arus masuk kalsium yang lambat, peningkatan konsentrasi digitalis berhubungan dengan peningkatan kalsium intraseluler yang memperlambat depolarisasi menyebabkan blok sinus. Blok AV juga disebabkan oleh akumulasi potasium di dalam sel dan sodium di luar sel. Infus bolus digoksin menginduksi terjadinya vasokonstriksi arteri koronaria epikardial, proses tersebut tidak diperantarai oleh aktivasi α adrenergik dan mudah dilawan oleh pemberian nitrat.
- Overdosis masif digitalis menyebabkan hambatan yang luas terhadap Na-K-ATPase termasuk pada jaringan non jantung, memperlambat konduksi dan menyebabkan re-entrant aritmia. Efek toksik digitalis pada kemoreseptor area postrema di medula SSP menyebabkan anoreksia, mual dan muntah.
- Korelasi yang buruk antara gejala klinik dan kadar toksik digitalis menyebabkan deteksi klinik terhadap terjadinya efek toksik menjadi sangat sulit. Konsentrasi serum digitalis yang pasti secara reguler harus dipantau; pasien dengan gagal jantung kongestif yang mendapat terapi digitalis mempunyai konsentrasi serum sekitar 1,4 ng/ml (1,8 nmol/L), dimana secara umum toksisitas digitalis terjadi pada tingkat 2 – 3 kali nilai tersebut. 50% kematian terjadi pada konsentrasi digitalis 6 ng/ml.
- Kuinidin meningkatkan kadar digitalis karena obat ini mula-mula menggeser digoksin dari ikatannya di jaringan. Tingginya kadar mantap terutama karena obat ini mengurangi bersihan ginjal sebanyak 40 – 50%. Perubahan yang timbul sebanding dengan tingginya dosis kuinidin, akan tetapi ada perbedaan individual dalam besarnya peningkatan. Pada umumnya kadar digoksin naik 2 kali, tetapi kisarannya dapat mencapai 4 kali. Kadar digoksin plasma mulai meningkat dalam waktu 24 jam setelah kuinidin diberikan dan mantap setelah 4 hari, setelah itu tetap tinggi kecuali bila dosis digoksin dikurangi. Bila digoksin dan kuinidin diberikan bersama, efek digoksin terhadap jantung dan SSP meningkat dan akhirnya dapat terjadi gejala-gejala keracunan. Oleh karena itu, pasien yang diobati sekaligus dengan digitalis dan kuinidin harus diawasi dengan cermat terutama gambaran EKG-nya, dan kadar digoksin plasma dimonitor hingga tercapai kadar mantap yang baru. Obat lain yang dapat menimbulkan interaksi yang mirip dengan kuinidin adalah kuinin, verapamil, diltiazem dan amiodaron.
- Antagonis β-adrenergik dan suksinilkolin meningkatkan aritmia pada pasien yang mendapat digitalis. Antagonis β-adrenergik dan digitalis menurunkan konduksi AV, berpotensi meningkatkan aritmia. Suksinilkolin cenderung meningkatkan secara cepat potasium serum dan meningkatkan aritmia oleh digitalis. Prokainamid sebagai zat antiaritmia dapat digunakan untuk terapi keracunan digitalis, juga berpotensi menimbulkan gangguan konduksi AV menyebabkan asistol atau fibrilasi ventrikel. Oleh karena hiperkalsemia mempengaruhi aritmia oleh digitalis, maka pemberian bolus cepat kalsium intraoperatif harus hati-hati pada pasien yang mendapat terapi digitalis jangka panjang. Beberapa obat potensial meningkatkan konsentrasi serum digitalis dengan cara menurunkan bersihan ginjal seperti antagonis saluran kalsium, spironolakton, amilorid dan triamteren. Hiper atau hipokalemia memperburuk toksisitas digitalis. Beberapa obat mengubah metabolisme digitalis ( menurunkan konsentrasi serum digitalis) dengan cara meningkatkan aktivitas enzim mikrosomal hepar, seperti phenilbutazon, phenobarbital, phenitoin dan rifampicin. Aminoglikosid menurunkan absorbsi digitalis oral.
- Pertanyaannya adalah seberapa besar pemberian digitalis pada pagi menjelang operasi. Oleh karena toksisitas digitalis berkorelasi dengan konsentrasi plasmanya, kadar digitalis harus dievaluasi saat preoperasi pada pasien yang mendapat preparat digitalis oral. Ada atau tidak adanya riwayat mual dan muntahharus dipastikan, sebab gejala tersebut dapat merupakan gejala keracunan digitalis walau konsentrasi serum digitalis “dalam batas normal” terapeutik. Mungkin tidak ada salahnya memberikan digitalis sesuai dosis yang biasa diberikan pada hari pembedahan sepanjang tidak ada bukti gejala keracunan. Betapapun demikian, jika konsentrasi serum digitalis meningkat, dosis pagi hari menjelang operasi harus diberikan secara hati-hati. Untuk kewaspadaan apakah digitalis akan diberikan pada hari operasi, maka konsentrasi serum potasium harus dipertahankan dalam batas normal saat perioperatif untuk mencegah terjadinya aritmia akibat obat tersebut.
VASODILATOR KORONARIA : NITRAT
- Penggunaan nitrat untuk terapi penyakit jantung iskemik dimulai sejak akhir tahun 1800-an. Nitrogliserin merupakan bahan aktif dinamit hasil penemuan Alfred Nobel, dimana dia sendiri menderita angina dan mendapat terapi nitrogliserin sampai akhir hayatnya. Para ahli anestesiologi menggunakan nitrovasodilator seperti nitrogliserin dan sodium nitroprusid selama lebih dari 20 tahun.
- Mekanisme kerja nitrat organik melalui pembentukan radikal bebas nitrogen oksida (NO) menstimulasi guanilat siklase sehingga kadar siklik-GMP dalam sel otot polos meningkat. Selanjutnya siklik-GMP menyebabkan defosforilasi miosin sehingga terjadi relaksasi otot polos.
- Nitrat organik menimbulkan relaksasi otot polos termasuk arteri dan vena. Pada dosis rendah nitrogliserin terutama menimbulkan dilatasi vena, sedangkan arteriol hanya sedikit dipengaruhi. Venodilatasi ini menyebabkan turunnya tekanan diastolik akhir (end-diastolic pressure) ventrikel kiri dan kanan. Resistensi vaskuler sistemik biasanya tidak berubah, frekuensi denyut jantung tidak berubah atau meningkat sedikit karena refleks, resistensi vaskuler paru dan curah jantung menurun. Pembuluh darah arteriol di wajah melebar (flushing) dan timbul sakit kepala berdenyut karena dilatasi arteri meningeal. Pada dosis tinggi dan pemberian cepat, nitrat organik menimbulkan venodilatasi dan dilatasi arteriol perifer sehingga tekanan sistolik maupun diastolik menurun, curah jantung berkurang, dan frekuensi jantung meningkat (refleks takikardia). Pasien akan tampak pucat, lemah dan mengeluh pusing. Aliran darah koroner meningkat sementara, tetapi kemudian menurun karena tekanan darah arteri dan curah jantung menurun. Efek hipotensi nitrat organik ini terutama terjadi pada pasien dalam posisi berdiri, karena darah semakin banyak berkumpul dalam vena sehingga curah jantung semakin menurun. Hipotensi juga terjadi bila obat diberikan berulang dengan interval pendek.
- Menghilangnya gejala angina pektoris pada pemberian nitrat organik diduga karena menurunnya kerja jantung dan perbaikan sirkulasi koroner. Nitrat organik memperbaiki sirkulasi koroner pada pasien aterosklerosis koroner bukan dengan cara meningkatkan aliran koroner total, tetapi dengan menimbulkan redistribusi aliran darah pada jantung. Daerah subendokard yang sangat rentan terhadap iskemia karena pembuluh darahnya mengalami kompresi tiap sistol akan mendapatkan perfusi lebih baik pada pemberian nitrat organik. Hal ini diduga karena nitrat organik menyebabkan dilatasi pembuluh darah koroner yang besar di daerah epikardial dan bukan pembuluh darah yang kecil (arteriol), sehingga tidak terjadi steal phenomenon yaitu suatu keadaan berkurangnya aliran darah di daerah iskemik karena terjadinya vasodilatasi pada daerah normal akibat pemberian vasodilator (arteriol), sehingga perfusi di jaringan sehat lebih baik. Pada jaringan yang iskemik terjadi vasodilatasi yang hampir maksimal karena di daerah tersebut berkumpul zat-zat bersifat asam yang menimbulkan dilatasi seperti laktat, fosfor inorganik (otoregulasi), sehingga pemberian vasodilator yang mempengaruhi tonus pembuluh darah kecil tidak bermanfaat. Sebaliknya, karena nitrat organik menimbulkan dilatasi pembuluh koroner yang besar (epikardial) maka redistribusi aliran darah ke daerah iskemik (yang berdilatasi akibat otoregulasi) menjadi lebih baik (dibandingkan dengan jaringan normal).
- Nitrat organik menurunkan kerja jantung melalui efek dilatasi pembuluh darah sistemik. Venodilatasi menyebabkan penurunan alir darah balik ke jantung, sehingga tekanan akhir diastolik ventrikel (beban hulu) dan volume ventrikel menurun. Beban hulu yang menurun juga memperbaiki perfusi subendokard. Vasodilatasi menyebabkan penurunan resistensi perifer sehingga beban hilir (tegangan dinding ventrikel sewaktu sistol) berkurang. Akibatnya, kerja jantung dan konsumsi oksigen menjadi berkurang. Ini merupakan mekanisme anti angina yang utama dari nitrat organik.
- Nitrat organik tidak mempengaruhi inotropi dan kronotropi jantung secara langsung, tetapi pada dosis tinggi aliran koroner dapat berkurang karena terjadinya refleks takikardi dan peningkatan kontraktilitas miokard. Hal ini dapat menimbulkan serangan angina paradoksal.
- Nitrogliserin sublingual cepat diabsorbsi oleh mukosa sublingual dengan mula aksi 2 – 5 menit, efek maksimal tercapai dalam waktu 3 – 15 menit, dan sebagian kecil sisanya masih aktif setelah 30 menit. Efek fisiologis semua nitrat ester sama seperti nitrogliserin, dengan variasi mula aksi dan lama aksi tergantung dari bentuk sediaannya. Nitrogliserin dan nitrat ester cepat dimetabolisme di hepar oleh enzim glutation organik nitrat reduktase, dan hasil metabolitnya tidak mempunyai aktivitas terhadap kardiovaskuler. Sediaan nitrat kerja panjang meliputi nitrogliserin oral (4 – 6 jam); salep nitrogliserin 2% (3 – 6 jam); isisorbid dinitrat sublingual (1,5 – 3 jam), oral (4 – 6 jam), tablet isap (2 – 3 jam); pentaeritriol tetranitrat oral (3 – 5 jam).
- Walaupun nitrat biasanya dapat ditoleransi dengan baik, efek samping yang paling sering berupa dizziness, sakit kepala dan postural hipotensi. Sesungguhnya tidak terdapat interaksi antara nitrat preoperatif dan agent anestetik sepanjang keadekuatan status volume dapat dipertahankan. Oleh karena terapi nitrat mempunyai toleransi yang baik, penghentian mendadak terapi nitrat akan menyebabkan iskemik miokard akut, sehingga terapi nitrat sebaiknya diteruskan selama masa perioperatif pada pasien-pasien yang biasa mendapat terapi tersebut.
- Pada otot jantung manusia lebih didominasi oleh reseptor β-adrenergik yaitu β1 dan β2. Terdapat pula reseptor α1-adrenergik dimana aktivitas peningkatan inotropiknya amat kecil. Peranan β-adrenergik adalah memperantarai respon inotropik miokard dan peningkatan laju jantung (kronotropik) terhadap katekolamin endogen dan eksogen termasuk katekolamin sintetik. Oleh karena peningkatan status inotropik dan laju jantung tersebut akan meningkatakan kebutuhan oksigen miokard (hal yang tidak dapat ditolerir pada pasien dengan penyakit arteri koroner). Antagonis β-adrenergik sering digunakan untuk menurunkan kebutuhan oksigen miokard menyeluruh dan selanjutnya dapat menurunkan frekuensi serangan angina.
- β-bloker efektif untuk pengobatan angina stabil kronik karena :
- (1) mengurangi kebutuhan oksigen miokard dengan cara mengurangi frekuensi laju jantung, kontraktilitas miokard dan tekanan darah (beban hilir) melalui penghambatan adrenoseptor –β di jantung sewaktu kerja fisik;
- (2) meningkatkan suplai oksigen miokard dengan cara mengurangi tegangan dinding ventrikel selama sistol (beban hilir), serta memperlambat laju jantung (waktu diastol memanjang) sehingga perfusi subendokard meningkat.
- Tidak semua efek β-bloker menguntungkan terhadap suplai dan kebutuhan oksigen miokard. β-bloker juga meningkatkan kebutuhan oksigen miokard melalui penurunan frekuensi laju dan kontraktilitas jantung sehingga meningkatkan waktu sistol (systolic ejection period) dan volume ventrikel (left ventricular end-diastolic volume). Selain itu, β-bloker juga mengurangi suplai oksigen miokard yang terjadi karena vasokonstriksi koroner akibat meningkatnya tonus α-adrenergik (unmasking effect). Akan tetapi sebagai hasil akhir, efek β-bloker adalah menurunkan konsumsi oksigen miokard, terutama selama kerja fisik. Berdasarkan efek farmakodinamik di atas, maka β-bloker bermanfaat untuk pengobatan angina stabil dan tidak berguna bahkan dapat memperburuk angina tak stabil karena vasospasme koroner.
Generic
Name
|
Trade
Name
|
Relative
β-AR Subtype
Receptor Selectivity
|
Usual Adult Dose
|
Maximum Adult Dose
|
Acebutolol
Atenolol
Esmolol
Metoprolol
Nadolol
Pindolol
Propranolol
Timolol
|
Sectral
Tenormin
Brevibloc
Lopressor
Corgard
Visken
Inderal
Blocadren
Timoptic
(eye drop)
|
β1-AR
β1-AR
β1-AR
β1-AR
Nonselective
Nonselective
Nonselective
Nonselective
|
200 – 800 mg total
(po) (qd/bid dosing)
50 – 100 mg qd (po)
5 – 10 mg (iv)
25 – 200 μg/kg/min (iv)
100 – 450mg qd (po)
5 – 15 mg (iv)
40 – 80 mg qd (po)
5 – 30 mg bid (po)
40 – 160 mg bid (po)
0,5 – 2 mg (iv)
10 – 20 mg bid (po)
|
1200 mg total
(po) qd/bid dosing
200 mg qd (po)
300 µg/kg/min (iv)
450 mg qd (po)
160-320 mg qd (po)
60mg/day total (po)
640mg/daytotal(po)
4 – 5 mg (iv)
60 mg/day total(po)
|
Note : This is not a complete list of beta-ARs.
qd=once daily; bi= twice daily; tid=three times daily; qid=four times daily.
- β-bloker yang kardioselektif mengurangi bahaya terjadinya bronkospasme pada pasien dengan gangguan jalan napas (misalnya asma bronkial dan penyakit paru obstruktif kronik) dan mengurangi terjadinya hipoglikemia pada pasien diabetes melitus. Tetapi kardioselektif ini sifatnya relatif, hanya ada pada dosis rendah, dan hilang pada dosis tinggi. Walaupun β-bloker yang kardioselektif atau mempunyai ISA (intrinsic sympathomimetic activity) kurang menimbulkan konstriksi bronkus, penggunaan obat-obat ini untuk penyakit bronkospastik (asma) harus dilakukan dengan sangat hati-hati.
- β-bloker dengan ISA atau aktivitas agonis parsial mengurangi terjadinya bradikardi istirahat. Sifat ini tidak bermanfaat bagi pasien dengan insufisiensi jantung, tetapi mempunyai keuntungan pada pasien dengan gangguan sirkulasi perifer. β-bloker dengan ISA kurang efektif untuk pengobatan angina stabil yang berat.
- Efek samping β-bloker kebanyakan merupakan kelanjutan dari efek farmakologiknya, yaitu akibat blokade adrenoseptor-β-adrenergik : bradikardi, blok AV, gagal jantung, bronkospasme dan lain-lain. Gagal jantung, walaupun jarang, dapat terjadi mendadak atau pelan-pelan, biasanya pada pasien dengan gangguan fungsi jantung.
- Efek samping β-bloker yang bukan kelanjutan efek farmakologiknya adalah : (1) efek pada saluran cerna : mual, muntah, diare ringan, konstipasi; (2) efek sentral : mimpi buruk, insomnia, halusinasi, rasa capai, pusing, depresi; dan (3) reaksi alergi : rash, demam dan purpura; bila timbul reaksi ini obat harus dihentikan.
- β-bloker dikontraindikasikan pada pasien dengan :
- (1) penyakit paru obstruktif, kecuali untuk asma ringan atau bronkitis kronik yang asimtomatik yang dangat memerlukan β-bloker, dalam hal ini dapat diberikan β-bloker yang kardioselektif bersama β2-agonis untuk mengatasi bronkokonstriksi yang mungkin terjadi;
- (2) diabetes melitus yang mudah terserang hipoglikemia pada pengobatan dengan insulin atau hipoglikemik oral;
- (3) penyakit vaskuler perifer yang berat (nekrosis kulit, klaudikasio yang memburuk);
- (4) disfungsi jantung yang sedang sampai berat, kecuali akibat hipertensi, aritmia atau takikardi sinus yang responsif terhadap β-bloker;
- (5) blok AV derajat 2 – 3; dan
- (6) sick sinus syndrome atau bradikardi.
- β-bloker harus diberikan dengan hati-hati pada pasien dengan :
- (1) diabetes melitus yang stabil (yang tidak mudah terserang hipoglikemia) : dapat diberikan β-bloker yang kardioselektif;
- (2) gangguan sirkulasi perifer yang ringan, dapat diberikan β-bloker dengan ISA atau β-bloker yang kardioselektif;
- (3) gagal jantung yang ringan, dapat diberikan β-bloker dengan ISA;
- (4) gangguan konduksi jantung yang ringan (derajat 1), dapat diberikan β-bloker dengan ISA.
- Pemberian β-bloker bersama digitalis dapat memberikan efek aditif dalam mendepresi konduksi AV sehingga dapat terjadi disosiasi AV dan henti jantung.
- Bila pemberian β-bloker hendak dihentikan, harus dilakukan secara bertahap sekurang-kurangnya 1 – 2 minggu, karena bila dihentikan mendadak dapat terjadi fenomena rebound, mengakibatkan angina makin memburuk sampai terjadi infark miokard. Sindrom ini tampaknya kurang terjadi pada β-bloker dengan ISA
ANTAGONIS KANAL KALSIUM
- Antagonis kanal Ca++ (calcium channel blocker, CCB) adalah sekelompok obat yang bekerja dengan menghambat masuknya ion Ca++ melewati slow channel yang terdapat pada membran sel (sarkolema). Struktur kimia CCB sangat berbeda satu sama lainnya. Obat ini pertama kali dilaporkan mempunyai efek kronotropik dan inotropik negatif oleh Hass dan Hartfelder (1962), yang terjadi karena terhambatnya arus masuk ion Ca++ ke dalam sel jantung. Nama lain yang biasa dipakai untuk golongan obat ini adalah calcium antagonist atau calcium entry blocker.
- Dihidropiridin (DHP) : nifedipin, nikardipin, felodipin, amlodipin, dll.
- Difenilalkilamin : verapamil, galopamil, tiapamil, dll.
- Benzotiazepin : diltiazem.
- Piperazin : sinarizin, flunarizin, dll.
- Lain-lain : prenilamin, perheksilin, dll.
- Golongan 1, 2 dan 3 menghambat secara selektif kanal Ca++ (90 – 100%) (Grup A), sedangkan kelompok lainnya menghambat kanal Ca++ (50 – 70%) dan kanal Na+ (Grup B). Uraian selanjutnya dibatasi pada ketiga prototipe CCB yakni nifedipin, verapamil dan diltiazem.
- Pada otot jantung dan otot polos vaskuler, ion Ca++ terutama berperan dalam peristiwa kontraksi. Meningkatnya kadar ion Ca++ dalam sitosol akan meningkatkan kontraksi. Masuknya ion Ca++ dari ruang ekstrasel (2mM) ke dalam ruang intrasel dipacu oleh perbedaan kadar (kadar Ca++ ekstrasel 10.000 kali lebih daripada kadar Ca++ intrasel sewaktu diastol) dan karena ruang intrasel bermuatan negatif.
- Pada otot jantung mamalia, masuknya ion Ca++ meningkatkan kadar Ca++ sitosol dan mencetuskan penglepasan ion Ca++ dalam jumlah cukup banyak dari depot intrasel (retikulum sarkoplasmik) sehingga aparat kontraktil (sarkomer) bekerja. Masuknya ion Ca++ terutama berlangsung lewat slow channel. Slow channel berbeda dengan fast Na channel yang melewatkan ion Na+ dari ruang ekstrasel menuju ruang intrasel dan dihambat oleh tetrodotoksin. Kanal Ca++ tidak dihambat olehnya.
- Secara umum ada 2 macam kanal kalsium pada membran sel eksitabel :
- (1) Voltage-operated (VOC) atau potential-dependent channel (PDC), yang terbuka oleh depolarisasi;
- (2) Receptor-operated channel (ROC), yang terbuka oleh norepinefrin atau neurotransmiter lain tanpa terjadi depolarisasi (2,9).
- VOC juga dibagi dalam 3 subtipe : L, N dan T atas dasar konduktansi dan sensitivitas kanal tersebut terhadap perubahan potensial. Dari ke-3 subtipe ini, hanya tipe L yang sensitif terhadap CCB. CCB terutama bekerja pada jantung dan otot vaskuler, karena pada kedua jaringan ini banyak terdapat tipe L. Kanal L terdiri dsari 5 subunit, yakni α1, α2, β, γ dan δ, dan reseptor CCB terdapat pada subunit α1. Nifedipin, verapamil dan diltiazem berikatan dengan subunit α1 di tempat yang berlainan tetapi berdekatan dan saling mempengaruhi.
- Untuk kontraksi, otot jantung memerlukan ion Ca++ yang masuk dari luar sel disamping ion Ca++ dari gudang intrasel, otot polos bergantung hampir seluruhnya pada ion Ca++ ekstrasel, sedangkan otot rangka tidak memerlukan ion Ca++ ekstrasel. Oleh karena itu CCB menghambat kontraksi otot polos dan otot jantung, tetapi tidak menghambat kontraksi otot rangka.
- Pada otot polos vaskuler terdapat 3 macam kanal Ca++ untuk kontraksi, yakni VOC, ROC dan SOC (stretch-operated channel). VOC (terbuka pada perangsangan saraf) dan ROC (terbuka pada perangsangan NE/Epi) menentukan tonus vaskuler oleh perangsangan ekstrinsik. SOC yang terbuka pada perangsangan otot sendiri (miogenik) menentukan tonus vaskuler basal (intrinsik). Ion Ca++ dalam sitoplasma akan berikatan dengan kalmodulin menimbulkan fosforilasi myosin light chain dan kontraksi.
- CCB jauh lebih aktif dalam menyebabkan dilatasi arteriol daripada dilatasi vena. Pada arteri besar VOC lebih sensitif terhadap CCB dibanding ROC. Akan tetapi pada arteriol, yang menentukan resistensi perifer, sensitivitas VOC terhadap CCB sama dengan ROC. Pada jantung, ion Ca++ ekstrasel selain diperlukan untuk kontraksi otot jantung, juga untuk pembentukan impuls SA dan AV. Dengan demikian, CCB menyebabkan efek inotropik negatif, kronotropik negatif dan penghambatan konduksi AV.
- Jadi CCB terutama bekerja pada otot polos vaskuler (menyebabkan dilatasi arteriol perifer dan koroner), otot jantung (menimbulkan efek inotropik negatif), nodus AV dan nodus SA (menyebabkan hambatan konduksi AV dan laju jantung).
- Berbagai CCB menunjukan aktivitas yang berbeda terhadap otot polos vaskuler dan terhadap jantung. Hanya golongan 2 (verapamil) dan golongan 3 (diltiazem) yang mempunyai efek hambatan yang bermakna terhadap nodus AV dan SA. Aktivitas hambatan CCB terhadap kontraksi otot polos vaskuler dibanding hambatannya terhadap kontraksi otot jantung disebut selektivitas vaskuler. CCB golongan DHP bersifat vaskuloselektif, artinya DHP lebih aktif menghambat kontraksi otot polos vaskuler dibanding kontraksi otot jantung, generasi yang baru mempunyai selektivitas yang lebih tinggi dibanding nifedipin.
- Sifat vaskuloselektif ini, disamping tidak adanya efek yang bermakna pada nodus AV dan SA, membawa keuntungan pada :
- Pengobatan hipertensi : menurunkan tahanan tepi tanpa efek samping pada jantung, dan relatif aman dalam kombinasi dengan β-bloker.
- Pengobatan angina : mengurangi serangan angina tanpa efek samping pada jantung, dan relatif aman dalam kombinasi dengan β-bloker.
- Gangguan fungsi jantung : lebih aman.
- Hambatan influks Ca++ melalui kanal Ca++ oleh CCB bersifat kompetitif. Efek ini dapat diatasi dengan pemberian larutan Ca++, agonis β1 (epinefrin, isoproterenol) atau glikosida jantung.
- Antagonis kalsium mengurangi kebutuhan oksigen miokard melalui :
- (1) vasodilatasi perifer (terutama arteriol) sehingga menurunkan afterload (semua antagonis kalsium : N lebih dari V lebih dari D);
- (2) pengurangan kontraktilitas miokard (V lebih dari D); dan
- (3) penurunan frekuensi laju jantung (D lebih dari V).
- Antagonis kalsium meningkatkan suplai oksigen miokard melalui
- (1) dilatasi langsung arteri apikardial (N lebih dari D lebih dari V) sehingga dapat mengatasi atau mencegah vasospasme koroner pada angina vasospastik;
- (2) penurunan tekanan darah (N lebih dari V lebih dari D) sehingga tegangan dinding ventrikel selama sistol (afterload) berkurang dan akibatnya perfusi subendokard meningkat;
- (3) dilatasi arteri epikardial disertai dilatasi arteriol koroner yang lemah (sehingga resistensi koroner hanya sedikit berkurang dan autoregulasi hanya sebagian dihambat) menyebabkan aliran darah miokard meningkat terutama di daerah iskemik, dimana arteriol berdilatasi paling lebar akibat autoregulasi yang masih berfungsi;
- (4) dilatasi stenosis eksentris pada arteri epikardial (yang ternyata belum berdilatasi secara maksimal) sehingga meningkatkan aliran darah di pasca stenosis (daerah yang iskemik); dan
- (5) penurunan laju jantung (D lebih dari V) sehingga memperpanjang waktu diastolik, dan dengan demikian meningkatkan perfusi subendokard.
- Tetapi antagonis kalsium meningkatkan kebutuhan oksigen miokard melalui
- (1) penurunan frekuensi laju jantung (D lebih dari V) sehingga memperpanjang waktu sistolik, dan dengan demikian meningkatkan kerja jantung; dan
- (2) pengurangan kontraktilitas miokard (V lebih dari D) sehingga memperbesar volume ventrikel (preload).
- Dari mekanisme di atas, jelaslah bahwa antagonis kalsium efektif untuk angina akibat vasospasme koroner maupun aterosklerosis koroner.
General
Class
|
Drug
Class
|
Example
Drug (Trade Name)
|
Mechanism of
Action at the
Calcium
Channel
|
Usual Adult
Dose
|
Maximum
Adult
Dose
|
Group A
Group A
Group A
Group B
Group B
|
Phenyl- alkyla- mines
Benzo- thiaze- pines
Dihy- dropy- ridines
Pipera- zines
Other types
|
Verapamil
(Calan, Isoptin)
Diltiazem
(Cardizem)
Nifedipine
(Procardia)
Nicardipine
(Cardene)
Nimodipine
(Nimotop)
Isradipine
Cinnarizine
Flunarizine
Lidoflazine
Phenylamine
Perhexiline
Bepridil
|
Frequency-depen dent block of cal- cium channels
Frequency-depen dent block of cal- cium channels
Blockade of cal- cium channels at rest
Nonselective blockade of slow calcium channels
Nonselective blockade of slow calcium channels
Bepridil also attaches to smooth muscle calmodulin
|
120 – 480 mg total SR divided qd or bid (po)
30 – 90 mg qid (po)
30 – 60 mg qd (po)
20 – 40 mg tid (po); IV loading dose : 10 – 15 mg/hr X 15 min
IV maintenance: 1 – 3 mg/hr
30 – 60 mg q4h (po) for sub- arachnoid hemorrhage
5-10 mg qd (po)
|
480 mg total SR (po)
360 mg total qd (po)
120 mg qd (po)
22,5 mg total qd (po)
|
Efek samping, kontraindikasi dan interaksi obat
- Efek samping CCB yang utama merupakan kelanjutan dari efek farmakologiknya pada pembuluh darah dan jantung, yakni
- (1) vasodilatasi berlebihan (N sangat lebih dari V lebih dari D);
- (2) efek inotropik negatif (V lebih dari D lebih dari N);
- (3) depresi konduksi AV (V lebih dari D sangat lebih dari N); dan
- (4) depresi nodus SA.
- Efek samping akibat vasodilatasi berlebihan berupa nyeri kepala berdenyut, pusing, muka merah, udem perifer, hipotensi, refleks takikardi dan palpitasi. Berkurangnya perfusi koroner akibat hipotensi berlebihan dan/atau meningkatnya kerja jantung akibat terjadinya takikardi dapat menimbulkan atau memperburuk serangan angina; ini dapat terjadi pada pemberian nifedipin dosis terapi.
- Efek inotropik negatif CCB tidak menjadi masalah bila fungsi jantung pasien baik, tetapi dapat menimbulkan gagal jantung pada pasien dengan gangguan fungsi jantung. Kemungkinan terjadinya gagal jantung ini lebih besar bila CCB diberikan bersama obat lain yang juga bersifat inotropik negatif, misalnya β-bloker. Depresi konduksi AV menimbulkan blok AV, terutama bila pemberian CCB dikombinasi dengan obat lain yang juga mendepresi konduksi AV, misalnya β-bloker atau digitalis. Depresi nodus SA dapat menimbulkan bradikardi sinus dan henti sinus.
- Efek samping saluran cerna (mual, muntah, konstipasi dan sebagainya) jarang terjadi, kecuali konstipasi oleh verapamil cukup sering dijumpai. Nifedipin dan dihidropiridin lainnya adalah CCB yang paling aman untuk pasien dengan gagal jantung, karena CCB golongan DHP bersifat vaskuloselektif. Golongan DHP juga paling aman untuk dikombinasi dengan digitalis atau β-bloker, karena DHP tidak berefek pada nodus AV. Tetapi kombinasi DHP dengan β-bloker dapat menimbulkan hipotensi berat dan/atau gagal jantung bila diberikan kepada pasien dengan resiko tinggi, yakni pasien dengan angina pektoris berat, aterosklerosis pada 3 pembuluh koroner (triple-vessel disease), gangguan fungsi jantung dan/atau riwayat infark miokard. Sebaliknya verapamil, karena efeknya terhadap otot jantung, nodus SA dan nodus AV, dikontraindikasikan pada gagal jantung yang berat (fraksi ejeksi kurang dari 30%), sick sinus syndrome, blok AV derajat 2 – 3, hipotensi (tekanan arterial sistolik kurang dari 90 mmHg) atau syok kardiogenik fluter/fibrilasi atrium dengan sindrom WPW. Kombinasi verapamil dengan β-bloker intravena juga merupakan kontraindikasi; demikian juga kombinasi CCB dengan digoksin bila terdapat toksisitas digitalis.
- Diltiazem, karena sifatnya yang hampir sama dengan verapamil, kontraindikasinya hampir sama pula. Kadar plasma siklosporin meningkat pada pemberian bersama D atau V. N dan D meningkatkan kadar plasma fenitoin. Kadar plasma teofilin ditingkatkan oleh N dan V. V juga meningkatkan kadar plasma karbamazepin. Semua interaksi ini tampaknya akibat hambatan enzim mikrosomal hati oleh V, D maupun N. Sebaliknya, pemberian bersama simetidin (penghambat enzim sitokrom P450) meningkatkan kadar plasma N dan D, tetapi tidak mempengaruhi farmakokinetik V.
- Pemberian rifampisin bersama verapamil sangat menurunkan kadar plasma verapamil; hal ini tampaknya akibat induksi enzim metabolisme verapamil oleh rifampisin. Tidak ada data untuk N dan D dengan rifampisin, tetapi interaksi yang sama diperkirakan akan terjadi.
PENGHAMBAT ANGIOTENSIN CONVERTING ENZYME
- Kaptopril adalah penghambat enzim konversi angiotensin (penghambat ACE) yang pertama ditemukan. Sejak itu telah dikembangkan banyak penghambat ACE lain, dan yang telah resmi beredar di Indonesia adalah enalapril, lisinopril, kuinapril, perindopril, ramipril, silazapril, benazepril, delapril dan fosinopril. Secara umum penghambat ACE dapat dibedakan atas yang bekerja langsung, yakni kaptopril dan lisinopril; dan yang bekerja tidak langsung (merupakan prodrug), yakni semua yang lainnya.
- Renin disekresi oleh sel jukstaglomerular di dinding arteriol aferen dan glomerulus kedalam darah bila perfusi ginjal menurun (akibat menurunnya tekanan darah atau adanya stenosis pada arteri ginjal), bila terdapat deplesi natrium (penurunan kadar natrium dalam tubuli ginjal), dan/atau bila terdapat stimulasi adrenergik (melalui reseptor β1).
- Renin, yang merupakan enzim proteolitik, akan memecah angiotensinogen, suatu α-globulin yang disintesis dalam hati dan beredar dalam darah, menjadi angiotensin I (AI). AI yang relatif tidak aktif akan dikonversi dengan cepat sekali oleh ACE yang terikat pada membran sel endotel yang menghadap ke lumen di seluruh sistem vaskuler, menjadi angiotensin II (AII) yang sangat aktif. AII bekerja pada reseptor di otot polos vaskuler, korteks adrenal, jantung dan SSP untuk menimbulkan konstriksi arteriol dan venula (efek pada arteriol lebih kuat), stimulasi sintesis dan sekresi aldosteron, stimulasi jantung dan sistem simpatis, dan efek di SSP berupa stimulasi konsumsi air dan peningkatan sekresi ADH. Akibatnya terjadi peningkatan resistensi perifer, reabsorbsi natrium dan air, serta peningkatan laju jantung dan curah jantung. Peningkatan tekanan darah ini mengaktifkan mekanisme umpan balik yang mengurangi sekresi renin.
- ACE juga adalah enzim kininase II yang mengaktifkan bradikinin. Bradikinin merupakan vasodilator arteriol sistemik yang poten, kerjanya melalui produksi EDRF (endothelial-derived relaxing factor) dan prostaglandin oleh sel-sel endotel vaskuler.
- Sistem RAA tidak berperan aktif dalam mempertahankan homeostasis tekanan darah pada subyek dengan volume darah dan kadar natrium yang normal, tetapi berperan penting dalam mempertahankan tekanan darah dan volume intravaskuler sewaktu terdapat deplesi natrium dan cairan.
- Penghambat ACE mengurangi pembentukan AII sehingga terjadi vasodilatasi dan penurunan sekresi aldosteron yang menyebabkan terjadinya ekskresi natrium dan air, serta retensi kalium. Akibatnya terjadi penurunan tekanan darah pada pasien hipertensi asensial maupun jipertensi renovaskuler. Kadar plasma AII dan aldosteron menurun, sedangkan kadar plasma AI dan aktivitas renin plasma (PRA) meningkat karena mekanisme kompensasi. Sekresi aldosteron, yang dipengaruhi oleh faktor-faktor lain disamping sistem renin-angiotensin mungkin kembali ke nilai awal pada terapi jangka panjang. Karena efek vasokonstriksi AII paling kuat antara lain pada pembuluh darah ginjal, maka berkurangnya pembentukan AII oleh penghambat ACE menimbulkan vasodilatasi renal yang kuat, sehingga terjadi peningkatan aliran darah ginjal.
- Penurunan tekanan darah oleh penghambat ACE disertai dengan penurunan resistensi perifer, tanpa disertai refleks takikardi. Penghambat ACE juga mengurangi tonus vena. Besarnya penurunan tekanan darah oleh penghambat ACE berbanding lurus dengan PRA awal, tetapi hanya pada pemberian akut, dan tidak pada pemberian kronik. Tampaknya kerja golongan obat ini tidak hanya melalui sistem RAA, tetapi juga melalui sistem kinin. Hambatan inaktivasi bradikinin oleh penghambat ACE meningkatkan bradikinin dan prostaglandin vasodilator sehingga meningkatkan vasodilatasi akibat hambatan pembentukan AII. Penghentian obat-obat ini secara mendadak tidak menimbulkan fenomena rebound.
- Penghambat ACE mengurangi volume dan tekan pengisian ventrikel kiri, tetapi juga meningkatkan curah jantung. Laju jantung dan tekanan darah akan menurun pada awalnya, sedangkan pada penggunaan jangka panjang alir darah ginjal meningkat.
Drug
|
Trade
Name
|
Mechanism of
Action
|
Total Daily
Dose
|
Half-life
(hours)
|
Duration of
Action (hours)
|
Captopril
Enalapril
Enalapri- lat
Lisinopril
Pentopril
Ramipril
Alacepril
Quinapril
|
Capoten
Vasotec
Vasotec
IV
Zestril
|
ACE inhibitor
ACE inhibitor
Active meta- bolit (diacid) of enalapril /
ACE inhibitor
ACE inhibitor
ACE inhibitor
ACE inhibitor
ACE inhibitor
ACE inhibitor
Vascular con- verting enzym inhibitor
|
25 – 100 mg (po) divided bid or tid
2,5 – 40 mg (po) divided qd or bid
1,25 mg q6h (iv) administered over 5 min
10 – 40 mg qd (po)
750 mg (po)
20 mg (po)
50 mg (po)
10 – 80 mg qd (po)
|
1,7
11
12,6
1,0
|
6 – 10
(Active meta- bolites)
18 – 30
(Active meta- bolites)
Clinical res- ponse seen within 15 min
18 – 30
(No active metabolites)
10 – 18
24 – 60
6 – 10
10 – 16
(Active meta- bolites)
|
Efek samping dan interaksi obat
- Batuk kering merupakan efek samping yang paling sering terjadi, insidensnya sampai 10 – 20%, lebih sering pada wanita dan pada malam hari. Efek samping ini bergantung pada besarnya dosis, dan reversibel bila obat dihentikan.
- Efek samping berupa rash dan gangguan pengecap lebih sering terjadi pada penggunaan kaptopril karena adanya gugus sulfhidril pada obat ini, yang tidak dimiliki oleh penghambat ACE lainnya. Sekitar 10% pasien yang mendapat kaptopril mengalami rash makulopapuler atau morbiliform. Reaksi dermatologik ini menghilang bila obat dihentikan atau tidak selalu muncul kembali bila obat diberikan lagi; beberapa rash eritematosus hilang meskipun obat diteruskan.
- Gangguan pengecap (disgeusia) terjadi pada kira-kira 7% pasien yang diberi kaptopril; gangguan ini bersifat reversibel, tetapi pemberian kaptopril mungkin perlu dihentikan bila terjadi anoreksia dan penurunan berat badan. Rash dan disgeusia lebih jarang terjadi bila digunakan dosis rendah (≤ 150 mg sehari).
- Udem angioneurotik, yang dapat terjadi pada penggunaan semua penghambat ACE, dapat cukup parah sampai menjadi fatal, tetapi hanya terjadi < 0,1%. Resiko udem ini meningkat pada pasien yang meneruskan obat meskipun sudah terjadi ulkus di mulut atau rash kulit (2,9). Dosis pertama penghambat ACE dapat menimbulkan hipotensi simtomatik yang berat, terutama pada pasien yang mengalami deplesi cairan akibat pemberian diuretik, diet rendah garam, atau dialisis, atau pada pasien yang hiponetremik. Untuk mengurangi efek samping ini, dosis dimulai serendah mungkin dan dinaikan perlaha-lahan, dosis pertama dan setiap kali peningkatan dosis diberikan sebelum tidur, dan sebaiknya dosis diuretik dikurangi atau dihentikan dulu beberapa waktu sebelum memulai penghambat ACE. Diuretik dapat diberikan kembali kemudian, bila diperlukan.
- Pada pasien dengan penyakit jantung koroner, hipotensi akut ini dapat mencetuskan serangan angina. Gagal ginjal akut yang reversibel dapat terjadi pada pasien dengan stenosis arteri ginjal pada kedua ginjal atau pada satu-satunya ginjal yang berfungsi, akibat berkurangnya kadar AII yang pada kondisi ini diperlukan untuk konstriksi arteriol glomerulus eferen dan mempertahankan filtrasi glomerulus yang cukup; pada pasien ini penghambat ACE I tidak boleh diberikan. Proteinuria (lebih dari 1 g/hari) jarang terjadi. Dulu banyak dilaporkan pada penggunaan kaptopril dosis tinggi sekali dan terutama terjadi pada pasien yang mempunyai penyakit parenkim ginjal. Demikian juga dengan neutropenia, efek samping ini juga jarang terjadi.
- Hiperkalemia yang bermakna secara klinik jarang terjadi pada pasien dengan fingsi ginjal normal. Resiko hiperkalemia meningkat bila obat-obat ini diberikan pada pasien dengan gangguan fungsi ginjal, atau diberikan bersama suplemen kalium atau diuretik hemat kalium.
- Penghambat ACE tidak menimbulkan efek samping metabolik pada penggunaan jangka panjang, yakni tidak mengubah metabolisme karbohidrat maupun kadar lipid dan asam urat dalam plasma. Penghambat ACE, disamping β-bloker, juga dapat mengurangi resistensi insulin, sehingga menjadi AH terpilih pada hipertensi dengan NIDDM atau dengan obesitas.
- Pada saat ini penghambat ACE menjadi AH terpilih pada hipertensi dengan nefropati diabetik. Diperkirakan bahwa dilatasi arteriol glomerulus eferen oleh penghambat ACE akan mengurangi perbedaan tekanan hidraulik pada pembuluh kapiler glomerulus sehingga dapat mengurangi kebocoran albumin yang menyebabkan kerusakan membran dasar glomerulus, sehingga dapat memperlambat proses terjadinya glomerulosklerosis diabetik.
- Efek hipotensi penghambat ACE dilawan oleh obat-obat AINS, terutama indometasin, melalui hambatan sintesis prostaglandin yang bersifat vasodilator yang berperan penting dalam aliran darah ginjal serta metabolisme air dan garam. Pada akhirnya AINS menyebabkan retensi natrium dan air, yang mengurangi efek hampir semua AH. Penghambat ACE tidak boleh diberikan pada kehamilan trisemester 2 dan 3 karena dapat menyebabkan gagal ginjal dan kematian pada foetus.
- Sistem renin-angiotensin teraktivasi selama tindakan anestesi dan pembedahan sebagai respon stres terhadap stimulus noxious (intubasi, insisi bedah, bypass kardiopulmonal). Hormon lain yang timbul sebagai respon stres adalh katekolamin, hormon antidiuretik, kortisol, endorfin, glukagon, hormon pertumbuhan, glukose, laktat dan piruvat. Penglepasan renin akut dapat merupakan mekanisme proteksi untuk mempertahankan volume darah selama terjadinya hipotensi. Walau demikian, aktivasi renin dapat terjadi oleh karena stimuli yang lain (misalnya insisi) menghasilkan respon yang berlebihan, dan ini amat berbahaya untuk pasien dengan fungsi miokard yang buruk, oleh karena terjadi peningkatan yang cepat terhadap afterload dan volume darah.
- Penggunaan penghambat ACE selama anestesi dan pembedahan masih kontroversial. Beberapa ahli anestesiologi meneruskan pemberian jangka panjang obat tersebut pada masa preoperasi hingga hari pembedahan, dan terapi diteruskan sesegera mungkin pasca bedah agar tercapai kesetabilan hemodinamik dan kemampuan miokard (terutama jika berhadapan dengan kasus iskemik miokard atau gagal jantung kongestif). Terdapat beberapa laporan yang menyebutkan bahwa pemberian penghambat ACE preoperasi tidak meningkatkan kesetabilan hemodinamik selama masa intraoperatif. Laporan tersebut melibatkan pasien-pasien sehat dimana kejadian hipotensi menjadi lebih sering dan berlangsung lebih lama setelah induksi. Kejadian hipotensi selama masa intraoperatif pada pasien yang mendapat penghambat ACE berhubungan dengan penumpulan respon simpatis. Walaupun efek tersebut menguntungkan pada pasien dengan penyakit jantung, pada pasien sehat, penumpulan respon simpatis tersebut berpotensi mengganggu respon simpatis normal pada saat induksi, intubasi dan stimulasi bedah. Yang harus diperhatikan pada kedua keadaan tersebut adalah status volume untuk mencegah episode hipotensi nyata. Oleh karena penumpulan respon simpatis dapat dicapai dengan zat yang lain (misalnya narkotik seperti fentanil) dan juga menguntungkan untuk tindakan smooth anesthetic (pada kenyataannya penggunaan “simpatolisis” masih kontroversial), penghambat ACE secara rutin tetap diberikan saat preoperatif untuk pasien-pasien yang mendapat obat tersebut untuk jangka panjang. Laporan terbaru menyatakan bahwa penghambat ACE mempunyai efek protektif terhadap ginjal pada tindakan nonpulsatile cold cardiopulmonary bypass. Oleh karena secara umum terdapat hubungan antara penghambat ACE dan gagal ginjal pada pasien dengan latar belakang penyakit ginjal, maka penghentian penghambat ACE harus dilakukan secara hati-hati pada pasien yang akan menjalani prosedur pembedahan dengan resiko cedera ginjal (misalnya pembedahan aneurisma aorta abdominal).
DIURETIK
- Ginjal adalah organ pengatur yang secara selektif menghemat dan mengekskresikan air dan berbagai campuran kimia. Ginjal mengeliminasi cairan sisa dan produk akhir metabolisme yang berbahaya seperti urea, sulfat, asam urin, fosfat, dan menghemat substansi-substansi yang diperlukan untuk kehidupan seperti air, glukosa, Na+, K+, Cl- dan bikarbonat. Ginjal juga mengatur tekanan darah, volume hemostasis, keseimbangan asam-basa dan keseimbangan Na-K, sehingga memperbaiki mikrosirkulasi, perfusi jaringan sebagaimana juga nutrisi sel.
- Darah yang masuk ke ginjal melalui arteri renalis akan difiltrasi oleh glomeruli menjadi urin (darah tanpa protein dengan berat molekul besar dan sel-sel darah), kemudian melintasi di berbagai bagian dari nefron (pertama tubulus proksimal, kemudian descending dan thick ascending loop of Henle, tubulus konvulsivus distal, dan terakhir di tubulus kolektivus). Sel-sel epitel nefron bersifat spesifik yang dilengkapi dengan transpoter ion khusus pada membran luminal (urine-side) dan basolateral (blood-side). Setiap bagian memperlihatkan mekanisme yang berbeda dalam mereabsorbsi air dan garam.
- Tubulus proksimal meresorbsi 60 – 70% sodium dan air hasil filtrasi. Sodium ikut ditranspor pula oleh substansi terlarut lainnya seperti glukosa, asam amino dan fosfat masuk ke dalam sel tubulus proksimalis. Membran basolateral mempertahankan keseimbangan rendahnya sodium urin-sel tubulus proksimal oleh pompa ion sodium keluar sel masuk ke darah melalui Na-K-ATPase. Bikarbonat juga berperan penting pada proses tersebut dengan menukar 3 molekul sodium. Air di dalam sel tubulus proksimal dipecah oleh karbonik anhidrase membentuk hidrogen dan hidroksida; molekul hidroksida ini kemudian bergabung dengan karbon dioksida (terbentuk dari pemecahan asam karbonik di urin, melintasi membran masuk ke dalam sel tubulus proksimal) membentuk bikarbonat, dimana ikut terbawa dari sel menembus membran basolateral dengan 3 molekul sodium. Sebagai bagian dari sistem bikarbonat, hidrogen juga ditranspor dari sel ke dalam lumen urin melalui pertukaran proton sodium-hidrogen. Hasil pertukaran dari sodium bikarbonat dan air menghasilkan perbedaan konsentrasi klorida untuk direabsorbsi.
- Tempat reabsorbsi berikutnya di sepanjang nefron adalah pada thick ascending limb of the loop of Henle. Di sini ikut ditranspor sodium-potasium-2 klorida (Na+-K+-2Cl-) terjadi di permukaan lumen sel oleh energi hasil dari Na-K-ATPase di permukaan basolateral sel. Hal tersebut menghasilkan lebih besar daripada keseimbangan konsentrasi potasium dan klorida dalam sel, dan memfasilitasi potasium dan klorida keluar melalui transpor ikutan basolateral. Potasium tetap tinggal di sel pada permukaan luminal, dan klorida pada permukaan basolateral, menghasilkan potensial positif transepitelial, yang akhirnya memfasilitasi reabsorbsi sodium paraseluler. Selanjutnya sodium diabsorbsi di ascending limb of the loop Henle oleh transpor ikutan dan melalui mekanisme paraseluler.
- Pada tubulus konvulsivus distal, sodium dan klorida diabsorbsi melalui suatu transpor ikutan sodium-klorida luminal netral. Aktivitas Na-K-ATPase, potasium dan klorida selalu berubah di membran basolateral.
- Tempat terakhir aksi diuretik pada nefron adalah di tubulus kolektivus. Di sini kanal sodium luminal terdapat pada sel-sel prinsipal (tipe sel yang dominan pada tubulus kolektivus) menyebabkan masuknya sodium pada waktu Na-K-ATPase pada membran basolateral bekerja. Perlintasan potasium pada membran luminal dan basolateral selalu berubah. Aldosteron menstimulasi sekresi potasium, reabsorbsi sodium dan mensekresi proton di tubulus kolektivus melalui reseptor aldosteron intraseluler. Tipe sel yang lain di tubulus kolektivus adalah sel intercalated, pompa proton dari sel ini ke lumen melalui proton-translocating ATPase sebagai bagian dari proses katalisasi oleh karbonik anhidrase. Di dalam sel ini, bikarbonat ditukar klorida pada membran basolateral. Oleh karena jalur inilah, penghambat karbonik anhidrase mempunyai beberapa efek di tubulus kolektivus yang cukup bermakna
Class of
Diuretic
|
Example
|
Site of Action in
Nephron
|
Mechanism(s) of Action
|
Carbonic anhy- drase inhibitors
Osmotic agents
Xanthines
m-Sulfamoyl- benzoic acids
Phenoxyacetic acids(mercurial)
Phenoxyacetic acids (nonmer- curial)
Aminopyrazo- linones
Pyrazine carbo- xamides
Chloride chan- nel blockers
Benzothiazides
Pteridine
Spirolactones
|
Acetazola- mide
Mannitol
Aminophy- line
Furosemide
Bumetanide
Piretanide
Merbaphen
Ethacrynic acid (l-cyste- ine form)
(-) Indacrinon
Muzolimine
Amiloride
Thiazides
Hydrothiazide
Metplazone
Triamterene
Spironolac- tone
|
Proximal tubule
Collecting tubule
Glomerulus
Glomerulus
Proximal tubule
(minor)
Thick ascending Loop of Henle
Thick ascending Loop of Henle
Thick ascending Loop of Henle
Proximal tubule
Collecting tubule
Thick ascending Loop of Henle
Proximal tubule
Distal convoluted tubule; idem
Collecting tubule
Collecting tubule
|
Blocks movement of sodium into the proximal tubule
Has osmotic effect
Increases vascular perfusion of glomerulus
Unknown mechanism
Binds to and inhibits Na+-K+-2Cl- cotransporter; furosemide at very high concentrations may inhibit the basolateral K+-Cl- cotranspoter
Binds to and inhibits Na+-K+-2Cl- cotranspoter
Ethacrynic acid may inhibit the basolateral K+-Cl- cotrans- porter
Inhibits basolateral K+-Cl- cotransporter
Blocks sodium-proton ex- change at supraclinical concentration
Inhibits luminal Na+ channel
Inhibits basolateral chloride channels
Has saluretic effects, poorly characterized
Inhibits Na+-Cl- cotransporter
Inhibits Na+-Cl- cotransporter
Inhibits luminal Na+ channel
Inhibits aldosterone receptor
|
- Oleh karena beberapa pasien mendapat terapi diuretik jangka panjang, seharusnyalah dipahami mekanisme dan tempat aksi dari tiap-tiap obat, sehingga jika mungkin tailor therapy dapat digunakan untuk meningkatkan aliran urin, dan kombinasi beberapa diuretik dengan tempat aksi yang berbeda dapat meningkatkan efektivitas pengobatan.
- Pada gagal jantung, berkurangnya volume darah arterial menyebabkan ginjal menahan air dan garam. Sistem renin-angiotensin-aldosteron pun dipacu sehingga terbentuk angiotensin II yang merangsang sekresi aldosteron yang akan menambah retensi natrium disertai pembuangan kalium. Semua ini menyebabkan retensi cairan pada pasien gagal jantung. Diuretik memacu sekresi NaCl dan air sehingga beban hulu berkurang dan gejala bendungan paru dan bendungan sistemik berkurang. Diuretik juga mengurangi volume ventrikel kiri dan tegangan dindingnya sehingga resistensi perifer menurun.
- Diuretik diketahui berinteraksi dengan banyak obat, seperti AINS (menghambat sintesa prostaglandin sehingga mengurangi efek loop diuretik), litium (deplesi sodium dari diuretik akan meningkatkan reabsorbsi litium yang berpotensi mencapai tingkat toksik), dan lipid endogen (terapi diuretik tiazid kronik dapat meningkatkan kolesterol total dan low dan very-low-density lipoproteins). Interaksi antara diuretik dan agent anestesi masih belum banyak diketahui. Terapi diuretik kronik dapat menyebabkan deplesi potasium, yang akan meningkatkan kejadian aritmia selama pengobatan penyakit jantung iskemik, terutama pada pasien yang mendapat digitalis. Terapi kronik diuretik juga menyebabkan penurunan volume darah efektif, dimana keadaan ini baru terlihat setelah induksi anestesi, sehingga harus diperhatikan status cairan dan level potasium pada pasien yang mendapat diuretik preoperatif
PENGOBATAN JANTUNG AKUT INTRAOPERATIF
- Seorang Cardivascular Anesthesiologist telah memahami sepenuhnya menghadapi pasien-pasien sakit kritis yang menjalani tindakan anestesi. Dalam hal ini termasuk pemberian obat-obat vasoaktif, memanipulasi resistensi vaskuler sistemik dan inotropik jantung, juga menangani efek samping akut agent farmakologik. Penggunaan obat-obat tersebut secara rasional tidak hanya perlu pemahaman yang kuat dari konsep suplai dan kebutuhan oksigen miokard, tetapi juga perlu memahami tentang hukum Starling, venous return, inotropik miokard, laju jantung dan resistensi vaskuler sistemik